
 O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中
O2作用下,先用NaClO将CN-离子氧化成CNO-,再在酸性条件下继续被NaClO氧化成N2和CO2。环保工作人员在密闭系统中 用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
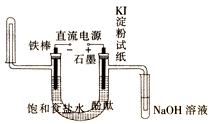
用下图装置进行实验,以证明处理方法的有效性,并测定CN-被处理的百分率。
 液全部放入乙中,关闭活塞。回答下列问题:
液全部放入乙中,关闭活塞。回答下列问题: 成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
成的气体除N2和CO2外,还有HCl及副产物Cl2等,上述实验是通过测定二氧化碳的量来确定对CN-的处理效果。则丙中加入的除杂试剂是__ __(填字母)
 验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。
验中戊中共生成0.82 g沉淀,则该实验中测得CN-被处理的百分率等于___ _____,请说明该测得值与实际处理的百分率相比偏高还是偏低_ ___?简要说明可能的原因________________________ _________ _________。 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.Cl2与Fe、Cu反应生成高价氯化物 |
| B.NH4HCO3晶体、固体I2受热均能变成气体 |
| C.SO2、Cl2均能使品红溶液褪色 |
| D.ClO-与Fe2+、H+均不能大量共存 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
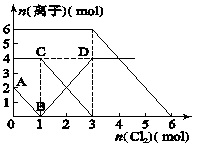
| A.原混合溶液中FeBr2的物质的量为6 mol |
| B.线段BD表示Fe3+物质的量的变化 |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硅是制造太阳能电池的常用材料 |
| B.NO、SiO2 ,SO3都可通过化合反应生成 |
| C.实验室可用NaOH溶液处理Cl2和SO2废气 |
| D.实验室可用浓硫酸干燥氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有①②③ | B.只有①② | C.只有②③ | D.只有①②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ____________________________ 。
____________________________ 。| A.①④②⑤③ | B.④①②⑤③ | C.②⑤④①③ | D.⑤②④③① |
 g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)
g次氯酸钙的同时,理论上需要消耗NaCl的物质的量为多少? (4分)查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。
应,反应完全后测得溶液中NaClO与NaClO3的物质的量之比为4:1。现有49.7g Cl2,将其通入到足量70℃的NaOH水溶液中,反应完全后得到500mL溶液。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的生成物是
氯化碘(ICl)的化学性质跟氯气相似,预计它跟水反应的生成物是
| A.HI和HClO | B.HCl和HIO | C.HClO3和HIO | D.HClO和HIO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com