
【题目】【化学﹣选修3物质结构与性质】 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物.
(1)基态硒原子的价层电子排布式为 .
(2)锗、砷、硒的第一电离能大小排序为 . H2SeO4的酸性比H2SeO3的强,其原因是 .
(3)H2SeO3的中心原子杂化类型是;SeO32﹣的立体构型是 . 与SeO42﹣互为等电体的分子有(写一种物质的化学式即可) .
(4)H2Se属于(填:极性或非极性)分子;单质硒的熔点为217℃,它属于晶体.
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为;若该晶胞密度为ρgcm﹣3 , 硒化锌的摩尔质量为M g/mol.NA代表阿伏加德罗常数,则晶胞参数a为pm. 
【答案】
(1)4s24p4
(2)As>Se>Ge;H2SeO4分了中非羟基氧数大于H2SeO3
(3)sp3;三角锥形;CCl4(或SiF4)
(4)极性;分子
(5)4;![]() ×1010
×1010
【解析】解:(1)硒为34号元素,有6个价电子,所以硒的价层电子排布式为4s24p4 , 所以答案是:4s24p4;(2)同一周期中,元素的第一电离能随着原子序数增大而呈增大趋势,但第ⅤA族元素第一电离能大于相邻元素,所以Ge、As、Se三种元素的第一电离能的大小顺序是:As>Se>Ge,含氧酸分子中非羟基氧越多,酸性越强,H2SeO4分了中非羟基氧数大于H2SeO3 , 所以H2SeO4的酸性比H2SeO3的强,
所以答案是:As>Se>Ge;H2SeO4分了中非羟基氧数大于H2SeO3;(3)H2SeO3的中心原子的价层电子对数为 ![]() =4,所以Se杂化方式为sp3杂化,SeO32﹣的中心原子Se的价层电子对数为
=4,所以Se杂化方式为sp3杂化,SeO32﹣的中心原子Se的价层电子对数为 ![]() =4,离子中有一个孤电子对,所以SeO32﹣的立体构型是 三角锥形,等电子体是指价电子和原子数都相等的微粒,与SeO42﹣互为等电体的分子有CCl4(或SiF4),
=4,离子中有一个孤电子对,所以SeO32﹣的立体构型是 三角锥形,等电子体是指价电子和原子数都相等的微粒,与SeO42﹣互为等电体的分子有CCl4(或SiF4),
所以答案是:sp3; 三角锥形;CCl4(或SiF4);(4)H2Se分子中有孤电子对,所以H2Se属于 极性分子,单质硒的熔点为217℃,比较小,所以它属于分子晶体,
所以答案是:极性;分子;(5)根据硒化锌晶胞结构图可知,每个锌原子周围有4个硒原子,每个硒原子周围也有4个锌原子,所以硒原子的配位数为4,该晶胞中含有硒原子数为8× ![]() +
+ ![]() =4,含有锌原子数为4,根据
=4,含有锌原子数为4,根据 ![]() =
= ![]() ,所以V=
,所以V= ![]() ,则晶胞的边长为
,则晶胞的边长为 ![]() cm=
cm= ![]() ×1010pm,
×1010pm,
所以答案是:4; ![]() ×1010 .
×1010 .


 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】当前,传统的塑料包装正日益被纸包装所取代,下述几种观点是对其原因的说明,其中正确的是( )
A.纸包装比塑料包装便宜
B.纸包装比塑料包装美观
C.纸包装比塑料包装更易制作
D.纸的主要成分是天然植物纤维素,容易被土壤微生物分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化学反应方程式正确的是( )
A.2﹣丙醇的催化氧化:2CH3CH(OH)CH3+O2 ![]() 2CH3CH2CHO+2H2O
2CH3CH2CHO+2H2O
B.用新制的Cu(OH)2悬浊液检验乙醛:CH3CHO+2Cu(OH)2 ![]() CH3COOH+Cu2O↓+2H2O
CH3COOH+Cu2O↓+2H2O
C.实验室制取酚醛树脂: 
D.甲醛溶液与足量的银氨溶液共热:HCHO+2[Ag(NH3)2]OH ![]() HCOONH4+2Ag↓+3NH3+H2O
HCOONH4+2Ag↓+3NH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中属于化学变化且吸热的是( )
①液态水汽化 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰⑥干冰升华
A. ①②B. ②④C. ③⑤D. ①⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中正确的是( )
①新制氯水久置后→浅黄绿色消失 ②Cl2通入石蕊试液中→先变红后褪色 ③SO2通入石蕊试液中→先变红后褪色 ④SO2通入品红溶液中→红色褪去 ⑤氨气通入酚酞溶液中→红色
A.①②③④
B.②③④⑤
C.①②④⑤
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从环己烷可制备1,4﹣环己二醇二醋酸酯,下列过程是有关的8步反应(其中所有无机产物都已略去):
(1)上述①~⑧8个步骤中
属于取代反应的是(填序号);
属于消去反应的是(填序号);
属于加成反应的是(填序号).
(2)写出下列物质的结构简式:
B , C , D .
(3)写出下列反应的化学方程式:
②;
⑤;
⑥ . 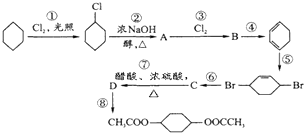
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW , 该温度下,将浓度为a mol/L的一元酸HA与b mol/L一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.混合溶液的pH=7
B.混合溶液中,c(H+)= ![]() mol/L
mol/L
C.a=b
D.混合溶液中,c(H+)+c(B+)=c(OH﹣)+c(A﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100 mL溶液中含H2SO4 0.50 mol,加入下列物质,溶液导电性增强的是( )
A.0.50 mol Ba(OH)2
B.100 mL水
C.0.50 mol酒精
D.0.50 mol Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com