
【题目】立足教材实验是掌握高中化学实验的基础,是理解化学科学的实验原理、实验方法和实验思路,提高学生实验能力的基本途径:
(1)实验1:取一块金属钠,在玻璃片上用滤纸吸干表面的煤油后,用小刀切去一端的外皮,观察钠的颜色,这个实验中还需用到的一种仪器是_________;
(2)实验2:向一个盛有水的小烧杯里滴入几滴酚酞试液,然后把一小块钠投入小烧杯,把反应的现象和相应结论填入空格,“浮”--钠的密度比水小;“红”--反应生成了氢氧化钠;“熔”——______________;
(3)实验3:用坩埚钳夹住一小块用砂纸仔细打磨过的铝,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是_________
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比倡的熔点高 D.打磨砂纸不能除去表面的氧化膜
(4)实验4:把少量水滴入盛有Na2O2固体的试管中,立即用带火星的木条放在试管口,检验
生成的气体体,向反应后的溶液中加入酚酞试液,可以看到__________;
(5)实验5:在玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,该氧化还原反应的氧化剂是__________,该反应每消耗1mol铁,转移电子的物质的量为_________。
(6)实验6:在试管中注入少量新制备的FeSO4溶液,用胶头滴管吸取NaOH溶液,将滴管尖端插入试管里溶液底部,慢慢挤出NaOH溶液,可以看到开始时析出一种白色的絮状沉淀,并迅速变成灰绿色,最后变成红褐色,发生这种颜也变化的原因是(用化学方程式表示):______。
【答案】 镊子 钠的熔点低,反应放热 BC 溶液先变红后褪色 水蒸气 8/3mol 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】本题考查实验方案设计与评价,(1)应用镊子夹取金属钠,因此还需要用到镊子;(2)熔是熔化,说明金属钠与水反应是放热反应,且金属钠的熔点较低;(3)熔化而不滴落,金属铝是活泼的金属,在空气中点燃产生一层致密的氧化薄膜,保护内部铝,熔化而不滴落,还说明氧化铝的熔点比铝高,故BC正确;(4)过氧化钠与水反应2Na2O2+2H2O=4NaOH+O2↑,酚酞与碱变红,又因为过氧化钠具有强氧化性,把有色物质氧化,因此溶液的颜色是先变红后褪色;(5)发生3Fe+4H2O(g) ![]() Fe3O4+4H2↑,氧化剂是化合价降低的物质,因此氧化剂是水蒸气,根据反应方程式,3molFe参与反应,转移电子物质的量为8mol,因此1molFe参与反应,转移电子物质的量为8/3mol;(6)氢氧化亚铁容易被氧化成氢氧化铁,反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
Fe3O4+4H2↑,氧化剂是化合价降低的物质,因此氧化剂是水蒸气,根据反应方程式,3molFe参与反应,转移电子物质的量为8mol,因此1molFe参与反应,转移电子物质的量为8/3mol;(6)氢氧化亚铁容易被氧化成氢氧化铁,反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L-1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤并转移
⑦定容 ⑧冷却 ⑨摇动
其正确的操作顺序为____________________。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、______________。
(2)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为________ g,要完成本实验该同学应称出________ g NaOH。
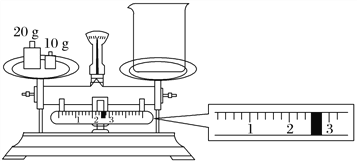
(3)使用容量瓶前必须进行的一步操作是____________________________________________。
(4)在配制过程中,其它操作都是正确的(按烧杯的实际质量),下列操作会引起误差偏低的是________。
A.转移溶液时不慎有少量洒到容量瓶外面
B.定容后塞上瓶塞反复倒转摇匀,静置后,液面低于刻度线,再加水至刻度线
C.称量时药品和砝码位置放反
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质和应用都正确的是
A.氢氟酸具有强酸性,可用于雕刻玻璃
B.氨气显碱性,可用碱石灰或无水CaCl2干燥
C.MgO、A12O3熔点高,它们都可用于制作耐火材料
D.铜的活动性比铁弱,可在海轮外壳装铜块减缓海轮腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一可自由滑动的隔板,将容器分成两部分。当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如右图所示位置(两侧温度相同)。则混合气体中CO和CO2的分子个数比为 ( )

A.1:1 B.1:3 C.2:1 D.3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的说法正确的是( )
A. 18个纵行代表18个族,7个主族、8个副族
B. 短周期共有32种元素
C. 元素周期表共有7个横行代表7个周期
D. 第ⅠA族全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择下列物质填空
(1)①蔗糖溶液 ②盐酸 ③NH3 ④熔融BaSO4 ⑤Fe(OH)3胶体 ⑥液态HCl ⑦NH3·H2O ⑧金刚石 ⑨Cu。能导电的物质是______________,电解质是______________,非电解质是____________。
(2)已知3.01×1024个氖原子的质量为w g,则氖气的摩尔质量是_________。
(3)将V1L 0.1mol/L NaOH溶液与V2L 0.3mol/L Ba(OH)2溶液混合,所得溶液OH-浓度为0.3mol/L,如果混合后体积为混合前的体积和,则V1︰V2= ____________。
(4)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有CO、CO2、O3三种气体,它们含有的氧原子个数之比为1:1:1,则这三种气体的物质的量之比为__________。
(2)1mol (NH4)2SO4所含的氮元素的质量与________gCO(NH2)2(尿素)所含的氮元素的质量相等。
(3)物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当它们的体积比为3∶2∶1时,三种溶液中Cl-的物质的量之比为________________。
(4)100 mL Al2(SO4)3溶液中c(SO42-)=0.9mol/L,则n[Al2(SO4)3]=____________。
(5)10 mL 6 mol/L 稀硫酸加水稀释到200 mL,稀释后c(H+)=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的数值,下列叙述正确的是
①标况下2.24L己烷中,含1.4NA个C-H键
②常温常压下,16gO2和O3混合气体中,电子数为8NA
③过氧化钠与水反应,产生3.2g氧气,则电子转移数目为0.2NA
④0.1mol/LKAl(SO4)2溶液中含Al3+数目小于0.1NA
⑤将0.1molFeCl3配成氢氧化铁胶体,胶体粒子数目最多可达到0.1NA
⑥将2.8gN2与足量氢气充分反应,得到氨气分子数目少于0.2NA
A. ①②④⑥ B. ③④⑤⑥
C. ②③⑥ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 金属钠投入水中:Na+H2O=Na++OH-+H2↑
B. 往酸性碘化钾溶液中滴加适量的双氧水:2I-+2H++H2O2=I2+2H2O
C. 往NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D. 氯气通入水中:Cl2+H2O![]() 2H++Cl-+ClO-
2H++Cl-+ClO-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com