
科目:高中化学 来源:2017届新疆乌鲁木齐地区高三第二次诊断性测验化学试卷(解析版) 题型:简答题
乙炔是一种重要的工业原料,由它制备人造橡胶——顺式聚异戊二烯的一种合成路线如下:
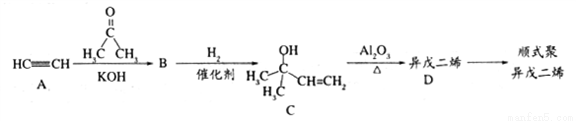
已知:在一定条件下可发生下列反应:
①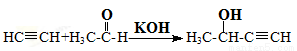 E
E
②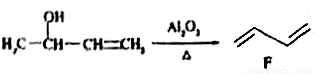
(1)乙醛的核磁共振氢谱中有______种峰,峰面积之比为_______。
(2)题给信息中反应②的反应类型是_____________。
(3)C中含氧官能团的名称是_______,D的系统命名法的名称是______。
(4)D分子中最多______个原子共面。
(5)下列物质能与E发生化学反应的是_______(填编号)。
a.溴水 b.酸性高锰酸钾 c.乙酸
(6)写出A→B的化学方程式_______。
(7)写出D生成顺式聚异戊二烯的化学方程式______________。
(8)写出与A物质具有相同官能团的异戊二烯的三种同分异构体结构简式_______、______、______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考试化学试卷(解析版) 题型:选择题
根据元素周期律,由下列事实进行归纳推测,推测不合理的是
选项 | 事实 | 推测 |
A | Mg与水反应缓慢,Ca与水反应较快 | Ba与水反应会更快 |
B | Si是半导体材料,同族的Ge也是半导体材料 | 第ⅣA族的元素的单质都可作半导体材料 |
C | HCl在1 500 ℃时分解,HI在230 ℃时分解 | HBr的分解温度介于二者之间 |
D | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:广西南宁市2017届高三第一次模拟测试理综化学试卷 题型:选择题
最近美国科学家实施了一项“天空绿色计划”,通过电解二氧化碳得到碳材料(部分原理如图所示),并利用得到的碳材料生成锂离子电池。下列说法正确的是

A. 图中能量转化方式只有一种
B. 阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑
C. 若反应中转移1mole-,则理论上消耗CO32-0.5mol
D. 当生成12g碳材料时,可收集到22.4LO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南师范大学附属中学高一3月月考化学试卷(解析版) 题型:填空题
(1)下列变化:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解。(填序号)
化学键没有被破坏的是________;仅发生离子键破坏的是_______ ; 仅发生共价键破坏的是________;既发生离子键又发生共价键破坏的是_______。
(2)已知1mol Si中含1mol Si—Si键。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/ kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①已知Si、SiC、SiO2熔化时必须断裂所含化学键,比较下列物质的熔点高低(填“>”或“<”):SiC________Si。
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)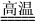 Si(s)+4HCl(g),则2 mol H2生成高纯硅需________(填“吸收”或“放出”)能量________kJ。
Si(s)+4HCl(g),则2 mol H2生成高纯硅需________(填“吸收”或“放出”)能量________kJ。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南师范大学附属中学高一3月月考化学试卷(解析版) 题型:选择题
右图为周期表中短周期的一部分,若a原子最外层电子数比次外层电子数少3个,下说法中不正确的是( )
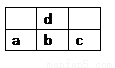
A. 原子半径大小顺序是c>b>d>a
B. d的氢化物比a的氢化物稳定
C. a和d的原子结合可以形成带3个负电荷的阴离子
D. a、b、c最高价氧化物对应水化物的酸性强弱关系是c>b>a
查看答案和解析>>
科目:高中化学 来源:2017届河北省石家庄市高三下学期模拟联考理科综合化学试卷(解析版) 题型:简答题
某工厂用一固体废渣(主要成份为Al2O3·Cr2O3,还含有FeO、SiO2)为主要原料回收利用,生产红矾钠晶体(Na2Cr2O7·2H2O),同时制备明矾(KAl(SO4)2·12H2O)。其主要工艺流程如下:
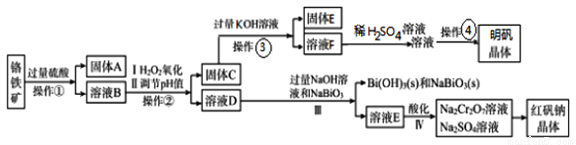
己知:NaBiO3不溶于冷水,在碱性条件下能将Cr3+氧化为CrO42-
(1)I、II目的是___________。
(2)实验室中操作④的名称为_______________。
(3)己知:Ksp[Fe(OH)3]=3.0×10-39,Ksp[Al(OH)3]=3×10-33。当pH=5.6时Cr(OH)3开始沉淀。室温下,II中需调节溶液pH范围为___________(杂质离子浓度小于1×10-6mol/L视为沉淀完全)。
(4)写出Ⅲ中发生反应的离子方程式_____________。
(5)IV中酸化是用硫酸而不用盐酸酸化,理由是_____________(结合化学方程式回答)。
(6)写出溶液F和硫酸溶液反应的离子方程式_________,若用足量二氧化碳通入F中,则生成的溶液中离子浓度关系为___________。
查看答案和解析>>
科目:高中化学 来源:2017届福建省厦门市高三下学期第一次质量检测理综化学试卷(解析版) 题型:选择题
某酸件废水可能含有Fe2+、Fe3+、Al3+、Mg2+、Na+、K+、CO32-、SO42-。取废水祥品分别进行如右图所示①~④四个实验。下列推断正确的是
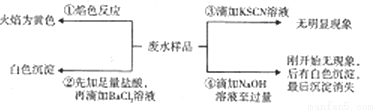
A. 废水含有Na+,不含K+
B. 废水含有SO42-和CO32-
C. 废水不含Fe3+,可能含Fe2+
D. 废水一定含有Na+、Al3+、SO42-
查看答案和解析>>
科目:高中化学 来源:山东省2016-2017学年高一3月月考化学试卷 题型:选择题
某元素X气态氢化物与该元素最高价氧化物的水化物反应生成盐,则该元素不可能具有的性质是.
A. 在周期表中处于第3周期VIIA B. 在周期表中处于第2周期VA族
C. 氢化物比PH3稳定 D. 常见化合价有-3、+2、+3、+5价
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com