
���ĸ������ͬ���ܱ������зֱ����һ������SO2��O2����ʼ��Ӧ�ǣ�������Ӧ�����ɴ�С��˳��������ȷ����
�ף��� 500��ʱ��SO2��O2�� 10 mol ��Ӧ
�ң���500��ʱ����V2O5��������SO2��O2��10 mol��Ӧ
������450��ʱ��8 mol SO2��5 mol O2��Ӧ
������500��ʱ��8 mol SO2��5 mol O2��Ӧ
| A���ҡ��ס������� | B���ҡ��ꡢ������ |
| C���ס��ҡ������� | D�����������ҡ��� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
2SO2+O2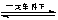 2SO3�ǽӴ��������Ṥ���е���Ҫ��Ӧ�����й��ڸ÷�Ӧ��˵���д������
2SO3�ǽӴ��������Ṥ���е���Ҫ��Ӧ�����й��ڸ÷�Ӧ��˵���д������
| A������SO2��Ũ���ܼӿ�÷�Ӧ������ |
| B��ͨ��ʹ���������� |
| C��������ϵ�¶Ȼ�����÷�Ӧ������ |
| D��ʹ�ô����ܸı�÷�Ӧ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ĸ���ͬ�������У��ֱ���в�ͬ�����µĺϳɰ���ӦN2(g)+3H2(g) 2NH3(g)������ͬʱ���ڱ�ʾ�÷�Ӧ����������
2NH3(g)������ͬʱ���ڱ�ʾ�÷�Ӧ����������
| A��v(H2)=0��1 mol/(L��s) | B��v(N2)=0��1 mol/(L��s) |
| C��v(N2)=0��2 mol/(L��s) | D��v(NH3)=0��3 mol/(L��s) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ס��������º��ݵ��ܱ������У��ֱ����һ������A��B��������Ӧ��A(g)��B(g) 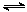 xC(g) ��H��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
xC(g) ��H��0�������������c(A)��ʱ��t�ı仯��ͼ��ʾ��
| ���� | �� | �� |
| �ݻ���L�� | 0.5 | 0.5 |
| ��Ӧ���ȣ�kJ�� | Q1 | Q2 |
| ��Ӧ����ʼ�� | 1 molA 1 molB | 0.5 molA 0.5 molB |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ������У�ʹ2 mol N2��6 mol H2��Ϸ������з�Ӧ:N2(g)+3H2(g) 2NH3(g)(����ӦΪ���ȷ�Ӧ)������˵���������
2NH3(g)(����ӦΪ���ȷ�Ӧ)������˵���������
| A������ƽ����ϵ���¶�(�����������)����������ƽ����Է���������� |
| B������ƽ����ϵ���¶�(�����������)�����������ܶȲ��䡡 |
| C������Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ��ǡ�1��3 |
| D�����ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���з�Ӧ�ﵽ��ѧƽ���ѹ�����¶���ʹ��ѧƽ�����淴Ӧ�����ƶ�����
A��SO2(g)+NO2(g)  SO3(g)+NO(g) ��H��0 SO3(g)+NO(g) ��H��0 |
B��C(s)+CO2(g)  2CO(g)��H��0 2CO(g)��H��0 |
C��4NH3(g)+5O2(g)  4NO(g)+6H2O(g)��H��0 4NO(g)+6H2O(g)��H��0 |
D��H2S(g)  H2(g)+S(s)��H��0 H2(g)+S(s)��H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
500�������£��ں����ܱ������У�����1molNO2��������ƽ��2NO2(g) N2O4(g) ��ƽ������������ٳ���1molNO2������˵����ȷ��
N2O4(g) ��ƽ������������ٳ���1molNO2������˵����ȷ��
| A��ƽ��������Ӧ�����ƶ� |
| B��ƽ�ⳣ��K���� |
| C��NO2��ת���ʱ�С |
| D��������������ɫ�ȱ�����dz������ԭ����Ҫdz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£������Ϊ10 L���ܱ������У�2 mol X��2 mol Y ���з�Ӧ��2X(g)+Y(g) Z(g)����2 min�ﵽƽ�⣬����0.6 mol Z������˵����ȷ����( )
Z(g)����2 min�ﵽƽ�⣬����0.6 mol Z������˵����ȷ����( )
| A����XŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.001 mol��L��1��s��1 |
| B�������������Ϊ20 L��Z��ƽ��Ũ��Ϊԭ����1/2 |
| C��������ѹǿ��������Y��ת���ʼ�С |
| D���������¶ȣ�X�������������,��÷�Ӧ�Ħ�H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com