
| ||
| ||
| ||
| ||


科目:高中化学 来源: 题型:
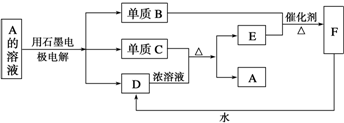
| A、pH:⑤>③>④>②>①>⑥ |
| B、c(A2-):⑤>②>④>①>⑥>③ |
| C、溶液中c(H+):⑥>①>④>②>③>⑤ |
| D、c(H2A):⑥>④>①>②>⑤>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③⑤ | C、①④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
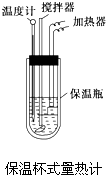 在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.
在量热计中将100mL 0.50mol?L-1的CH3COOH溶液与100mL 0.55mol?L-1的NaOH溶液混合,温度从298.0K升高至300.7K.已知量热计的热容常数(量热计各部件每升高1K所需要的热量)是150.5J?K-1,溶液密度均为1g?mL-1,生成溶液的比热容c=4.184J?(g?K)-1.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 |
| B、做本实验的当天室温较高 |
| C、将50mL 0.55mol?L-1的氢氧化钠溶液取成了50mL 0.55mol?L-1的氨水 |
| D、在量取盐酸时仰视读数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com