
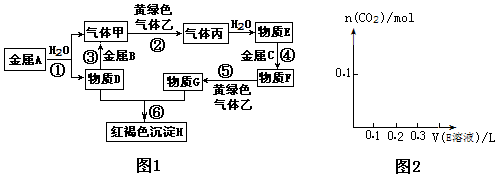
分析 A的一种氧化物具有强氧化性,可用作呼吸面具和潜水艇的供氧剂,为过氧化钠,则A为Na,由转化关系可知甲为H2,D为NaOH,则B为Al,黄绿色气体乙为Cl2,丙为HCl,E为盐酸,红褐色沉淀为Fe(OH)3,则G为FeCl3,C为Fe,F为FeCl2,以此解答该题.
解答 解:(1)三种金属分别为Na、Al、Fe,还原性最强的为Na,故答案为:Na;
(2)D为NaOH,可用焰色反应检验钠离子,故答案为:进行焰色反应;
(3)氯化亚铁与氢氧化钠反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成氢氧化铁,现象是得到白色沉淀迅速变灰绿色,最终变成红褐色,
故答案为:得到白色沉淀迅速变灰绿色,最终变成红褐色;
(4)铝和氢氧化钠溶液反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(5)F为氯化亚铁,具有还原性,可与硝酸发生氧化还原反应,反应的离子方程式为3Fe2++NO3-+4H+-=3Fe3++NO↑+2H2O,
故答案为:3Fe2++NO3-+4H+-=3Fe3++NO↑+2H2O;
(6)将红褐色沉淀H加热后得到的一种氧化物.该氧化物为氧化铜,与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾).同时还生成KNO2和H2O,方程式为,
故答案为:Fe2O3+3KNO3+4KOH$\frac{\underline{\;高温\;}}{\;}$2K2FeO4+3KNO2+2H2O
(7)D为NaOH,n(NaOH)=0.3mol,n(CO2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,反应后溶液为0.1mol碳酸钠、0.1molNaOH,加入HCl,先发生NaOH+HCl=NaCl+H2O,再以此发生Na2CO3+HCl=NaHCO3+NaCl、NaHCO3+HCl=NaCl+CO2+H2O,最后生成0.1mol二氧化碳,图象为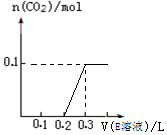 ,
,
故答案为: .
.
点评 本题综合考查无机物的推断,为高考常见题型,侧重于学生的分析能力和计算能力的考查,注意把握物质的性质以及反应的现象,把握推断题的突破口,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | S→SO3可以一步实验 | |
| B. | S是淡黄色固体,易溶于水 | |
| C. | Fe+S→FeS,Fe+Cl2→FeCl3,说明氧化性:Cl2>S | |
| D. | 试管壁上残留的S可以用酒精清洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | CO2通入NaClO 溶液中能生成HClO |
| B | 根据溶液的pH与溶液碱性的关系 | pH=6.8的溶液一定显酸性 |
| C | 组成和结构相似的物质,沸点随相对分子质量增大而升高 | H2O沸点低于H2S |
| D | 同主族元素从上至下非金属性减弱 | HF、HCl、HBr、HI的酸性依次减弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体区别于其它分散系的本质特征是分散质微粒直径在10-9 m~10-7m之间 | |
| B. | 用聚光手电筒照射CuSO4溶液和Fe(OH)3胶体时,产生的现象相同 | |
| C. | 将5-6滴饱和FeCl3溶液加入到沸水中继续加热至溶液呈红褐色制得了Fe(OH)3胶体 | |
| D. | Fe(OH)3胶体能够吸附水中悬浮的固体颗粒并沉降,达到净水目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯、苯和乙酸均能发生加成反应 | |
| B. | 某芳香烃的分子式为C10H14,它可使酸性 KMnO4溶液褪色,且分子结构中只有一个侧链,符合条件的烃有4种 | |
| C. | 1 mol的有机物(结构如图)最多能与含5mol NaOH的水溶液完全反应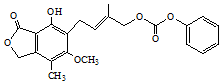 | |
| D. | 油脂皂化反应得到高级脂肪酸与甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极反应为:2H2+4OH--4e-═4H2O | |
| B. | 正极反应为:O2+4H++4e-═2 H2O | |
| C. | 电池工作时溶液中的阴离子移向正极 | |
| D. | 电池工作时负极区pH升高,正极区pH下降 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入铝粉有大量氢气产生的溶液中:Ca2+、K+、NO3-、Cl- | |
| B. | PH=0的无色溶液中:Na+、K+、MnO4-、NO3- | |
| C. | 在0.1mol/L的盐酸中:Fe2+、Na+、ClO-、Ca2+ | |
| D. | 在含有大量Fe3+的溶液中:NH4+、Ca2+、Cl-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com