
| ||
| m |
| M |
| n |
| V |
| 44.2g |
| 2 |
| ||
| 16.8g |
| 84g/mol |
| 5.3g |
| 106g/mol |
| 0.3mol |
| 0.6L |


科目:高中化学 来源: 题型:
| c(OH-) |
| c(H+) |
| Fe3+ | Al3+ | Fe2+ | Mg2+ | |
| 开始沉淀时 | 1.5 | 3.3 | 6.5 | 9.4 |
| 沉淀完全时 | 3.7 | 5.2 | 9.7 | 12.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NaHCO3=Na2CO3+CO2↑+H2O |
| B、2KMnO4=K2MnO4+MnO2+O2↑ |
| C、Ca(OH)2+CO2=CaCO3↓+H2O |
| D、Cu(OH)2+H2SO4=CuSO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100mL 3mol/L KCl溶液 |
| B、25mL 2mol/L AlCl3溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、25mL 1.5mol/L MgCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100 g?mol-1 |
| B、27.5 g?mol-1 |
| C、55 g?mol-1 |
| D、16.5 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、290 | B、282 |
| C、280 | D、278 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、互为同位素的原子性质几乎完全相同 |
| B、丙氨酸CH3-CH(NH2)-COOH存在手性异构体 |
| C、标准状况下,相同体积的NH3、CH4、HF含有相同的电子数 |
| D、等体积的NO和O2混合后所得的混合气体的平均摩尔质量为41.33 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、甲烷与氯气反应制氯仿:CH4+3Cl2
| ||
B、烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2
| ||
C、甲烷、CO合成乙酸乙酯:2CH4+2CO
| ||
D、乙烯合成聚乙烯nCH4+2CO
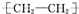 |
查看答案和解析>>
科目:高中化学 来源: 题型:
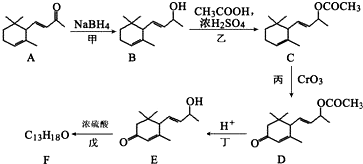
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com