
| NaOH/H2O |
| NaOH/�� |
| ���� |
| ���� |
| Br2 |
| NaOH/�� |
| ���� |
| ��ˮ |
| NaOH/ˮ |
| ���� |
| O2���� |
| ���� |
| O2���� |
| ���� |

| Cu |
| �� |
| Cu |
| �� |
 ��
�� ��
��


 ���ɶ��ȫ���ƿؾ�ϵ�д�
���ɶ��ȫ���ƿؾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ԭ��������ƽ��Ħ������Ϊ23.2g/mol |
| B�����������Na2O2��Ӧ�����е���ת�Ƶ����ʵ���Ϊ0.25mol |
| C����Һ��SO32-�����ʵ���Ũ�Ȼ������ֲ��� |
| D����Һ��HCO3-�����ʵ���Ũ�ȼ�С��CO32-�����ʵ���Ũ��������HCO3-��CO32-�����ʵ���Ũ��֮�ͻ������ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4+��NO3-�� CO32-��Na+ |
| B��Na+�� Ba2+�� Mg2+�� HCO3- |
| C��NO3-��Mg2+�� K+�� Cl- |
| D��NO3-��K+��AlO2-��OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢۢ� | B���ڢۢܢޢ� |
| C���ۢܢ��� | D���ڢݢߢ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
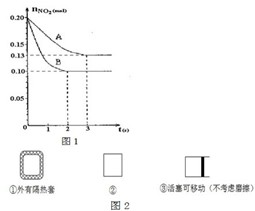 ���ݻ�ΪVL���ܱ������з���2NO2?2NO+O2��Ӧ����Ӧ������NO2�����ʵ�����ʱ��仯��״����ͼ1��ʾ��
���ݻ�ΪVL���ܱ������з���2NO2?2NO+O2��Ӧ����Ӧ������NO2�����ʵ�����ʱ��仯��״����ͼ1��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A��Al��Mg��OH��2��Si��S��Cu |
| B��Al��Fe��Mg��Si��Cu |
| C��Al2O3��SiO2��Fe��C��Cu |
| D��Al��Si��C��CuO��Cu |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ɱ����Ȼ��ơ����ʯ |
| B�������ơ��ռ�������� |
| C��NaCl��KCl��CsCl |
| D��H2O��H2S��H2Se��H2Te |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ħ�������͵������ʵ�ʽ�� |
| B��Ħ��������������ʽ����6.02��1023�� |
| C��HNO3��Ħ��������63 g |
| D��CaCO3��KHCO3��Ħ����������100 g?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+��Ba2+��Cl-��NO3- |
| B��SO32-��Cl-��Na+��SO42- |
| C��NH4+��K+��NO3-��SO42- |
| D��Al3+��Cl-��Na+��AlO2- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com