
【题目】磷化氢(PH3)是一种剧毒气体,是常用的高效熏蒸杀虫剂,也是一种电子工业原料.
(1)在密闭粮仓放置的磷化铝(AIP)片剂,遇水蒸气放出PH3气体,化学方程式为 ______
(2)利用反应PH3+3HgCl2=P(HgCl)3↓+3HCl,通过测定溶液 ______ 变化,可准确测定空气中微量的PH3;其中HgCl2溶于水,所得溶液几乎不导电,则HgCl2属于 ______ (填“共价”或“离子”)化合物.
(3)工业制备PH3的流程如图1所示:

①亚磷酸属于 ______ 元酸;
②当反应I生成的n(NaH2PO2):n(Na2HPO3)=3:1时,参加反应的n(P4):n(NaOH)= ______ .
(4)用漂白粉可将PH3氧化为H3PO4,化学方程式为 ______ ;含有水蒸气时可加快PH3的氧化过程,用离子方程式表示原因: ______ .
(5)从(4)中的反应产物中回收磷酸氢钙(CaHPO4)的方法如图2:
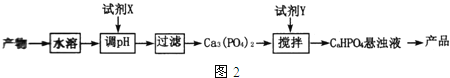
①试剂X为 ______ (填化学式);
②已知25℃时,H3PO4的Ka1=7.5×10-3、Ka2=6.3×10-8、Ka3=4.4×10-13.
CaHPO4悬浊液pH ______ 7(填“>”、“=”或“<”),通过计算说明理由 ______ .
【答案】AlP+3H2O=Al(OH)3+PH3 PH或电导率 共价 二 3:10 2Ca(ClO)2+PH3=H3PO4+2CaCl2 ClO-+H2OHClO+OH- Ca(OH)2或CaO > 水解常数Kh=1.59×10-7>Ka3=4.4×10-13,水解程度大于电离程度,溶液呈碱性
【解析】
⑴根据题意写出反应方程式。
⑵根据已知信息,检验空气中微量的磷化氢主要是看溶液的pH值或电导率,HgCl2溶于水,所得溶液几乎不导电,说明不存在离子,因此在溶液中不电离则为共价化合物。
⑶根据甲足量氢氧化钠溶液得到NaH2PO2得出亚磷酸为二元酸;根据化合价升降守恒和生成的产物中质量守恒分析得出白磷和氢氧化钠的物质的量之比。
⑷根据氧化还原反应原理书写化学方程式,次氯酸要水解生成的次氯酸更快的与磷化氢反应。
⑸磷酸被氢氧化钙或氧化钙反应生成磷酸钙,CaHPO4溶液中水解程度大于电离程度,因此溶液显碱性。
⑴磷化铝(AlP)片剂,遇水蒸气放出PH3气体,化学方程式为AlP+3H2O=Al(OH)3+PH3,故答案为:AlP+3H2O=Al(OH)3+PH3。
⑵HgCl2溶于水,所得溶液几乎不导电,发生反应PH3+3HgCl2=P(HgCl)3↓+3HCl,氯化氢易溶于水,所以可以通过测定溶液pH或电导率变化,准确测定空气中微量的PH3。HgCl2溶于水,所得溶液几乎不导电,说明不能电离出离子,因此HgCl2属于共价化合物,故答案为:pH或电导率;共价。
⑶①根据在足量的NaOH溶液作用下生成的亚磷酸钠的化学式得出亚磷酸属于二元酸,故答案为:二。
②当反应I生成的n(NaH2PO2):n(Na2HPO3) = 3:1时,假设n(NaH2PO2) = 3 mol,n(Na2HPO3) = 1 mol,则化合价升高+1×3 + (+3)×1 = 6,白磷中磷的化合价降低变为PH3,一个磷降低3个价态,需要2mol磷降低,因此总消耗磷的物质的量为3+1 + 2 = 6mol,即白磷1.5 mol,消耗氢氧化钠物质的量为3mol×1 + 1mol×2 = 5mol,因此参加反应的n(P4):n(NaOH) = 1.5:5 =3:10,故答案为3:10。
⑷用漂白粉可将PH3氧化为H3PO4,化学方程式为2Ca(ClO)2+PH3=H3PO4+2CaCl2,含有水蒸气时可加快PH3的氧化过程,次氯酸钙水解生成次氯酸,次氯酸具有更强的氧化性,可以更快地氧化磷化氢,因此离子方程式表示原因为ClO- + H2O HClO + OH-,故答案为:2Ca(ClO)2+PH3= H3PO4+ 2CaCl2;ClO- + H2O HClO + OH-。
⑸①试剂X主要是将磷酸等物质转变为磷酸钙,因此X试剂主要是Ca(OH)2或CaO,故答案为:Ca(OH)2或CaO。
②CaHPO4悬浊液中有HPO32-,HPO32-既能电离,也能水解,电离常数为H3PO4的第三步电离常数,即Ka3=4.4×10-13,水解常数Kh=![]() =
=![]() =1.59×10-7>Ka3,所以主要是水解为主,因此CaHPO4悬浊液pH >7,故答案为:>;水解常数Kh=1.59×10-7>Ka3=4.4×10-13,水解程度大于电离程度,溶液呈碱性。
=1.59×10-7>Ka3,所以主要是水解为主,因此CaHPO4悬浊液pH >7,故答案为:>;水解常数Kh=1.59×10-7>Ka3=4.4×10-13,水解程度大于电离程度,溶液呈碱性。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性。下列叙述中不正确的是:
A. 红热的铜丝在氯气中剧烈燃烧,生成棕黄色烟
B. 钠在氯气中燃烧,生成白色的烟
C. 纯净的氢气在氯气中安静的燃烧,在集气瓶口形成白色烟雾
D. 氯气能与水反应生成盐酸和次氯酸,次氯酸见光易分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物,用7.0 mol/L的盐酸100 mL在一定条件下恰好完全溶解,所得溶液中再通入0.56L标况下的Cl2时,刚好使溶液中的Fe2+全部转化为Fe3+,则该氧化物中Fe2+与Fe3+的物质的量之比为
A.1:4B.2:1C.4:1D.3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源。海水综合利用的部分流程图如下:
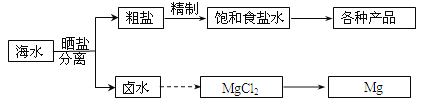
回答下列问题:
(1)用NaCl做原料可以得到多种产品
①工业上由NaCl制备金属钠的化学方程式是________________。
②实验室用惰性电极电解200mLNaCl溶液,若阴阳两极均得到224mL气体(标准状况),则所得溶液的pH为_________(忽略反应前后溶液的体积变化)。
③电解氯化钠稀溶液可制备“84”消毒液。“84”消毒液的有效成分为______,制取它的化学方程式为__________________________。
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。从卤水中提取镁的步骤为:
a.将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
b.将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
c.在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl26H2O;
d.将MgCl26H2O在一定条件下可以得到无水MgCl2;
e.电解熔融的MgCl2可得到Mg。
①上述提取镁的流程c中,得到MgCl2溶液的离子方程式为______________。
②步骤d中的“一定条件”指的是___________________。
③有同学认为:步骤b后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则。你同意该同学的想法吗?__________(填“同意”或“不同意”),请说出你同意或不同意的理由______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学实验中常见的制备气体并进行某些物质的检验和性质实验的装置,A是制备气体的装置,C、D、E、F中盛装的液体可能相同,也可能不同。试回答:
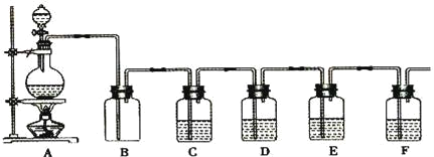
(1)如果A中的固体物质是碳,分液漏斗中盛装的是浓硫酸,试写出发生的化学反应方程式:____,若要检验生成的产物,则B、C、D、E、F中应分别加入的试剂为__、__、__、__、__,E中试剂和C中相同,E中试剂所起的作用__,B装置除可检出某产物外,还可起到__作用。
(2)若进行上述实验时在F中得到10.0 g固体,则A中发生反应转移的电子数为__个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)P2O5是非氧化性干燥剂,下列气体不能用浓硫酸干燥,可用P2O5干燥的是______
a.NH3 b.HI c.SO2d.CO2
(2)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1∶1。写出该反应的化学方程式:__________
(3)工业生产甲醇的常用方法是:CO(g)+2H2(g)![]() CH3OH(g) △H = —90.8kJ/mol。
CH3OH(g) △H = —90.8kJ/mol。
已知:2H2(g)+O2(g)=2H2O(l) △H = -571.6kJ/mol;
2CO(g)+O2(g)=2CO2(g) △H = -566.0kJ/mol
计算2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) △H =________。
(4)某实验小组设计了如图所示的甲醇燃料电池装置。
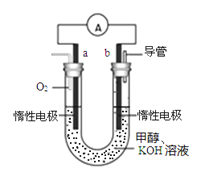
①该电池工作时,负极是_______极(填“a”或 “b”);
②工作一段时间后,测得溶液的pH减小,该电池负极反应的离子方程式为_________________。
(5)电解法促进橄榄石(主要成分是Mg2SiO4)固定CO2的部分工艺流程如下:
已知:Mg2SiO4(s)+4HCl(aq)![]() 2MgCl2(aq)+SiO2(s)+ 2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2(s)+ 2H2O(l) △H =-49.04 kJ·mol-1
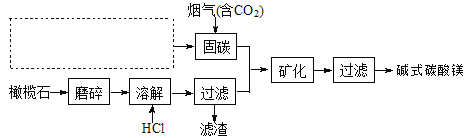
①某橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为_____________。
②在上图虚框内补充一步工业生产流程______________。
③经分析,所得碱式碳酸镁产品中含有少量NaCl和Fe2O3。为提纯,可采取的措施依次为:对溶解后所得溶液进行除铁处理、对产品进行洗涤处理。判断产品洗净的操作是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】橙花叔醇是一种具有香气的有机化合物,可用于配制玫瑰型、紫丁香型等香精,其结构如图所示,下列相关说法正确的是

A. 橙花叔醇的分子式为C15H24O
B. 橙花叔醇能发生氧化、还原、取代、聚合等类型的反应
C. 橙花叔醇与钠和NaOH均能发生反应
D. 橙花叔醇的同分异构体中可能含有苯环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素,e、g、h、i、j均是由这些元素组成的二元化合物,i常温常压下为液体,其余均为无色气体。e的摩尔质量为g的2倍,f是元素Z的单质,g物质能使湿润的红色石蕊试纸变蓝,h的组成元素位于同一主族。上述物质的转化关系如图所示。下列说法正确的是
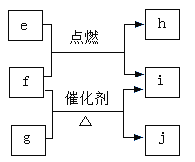
A.原子半径:Y>Z>W>XB.热稳定性:i>g, 沸点:i>e
C.Y与W的含氧酸均是强酸D.h与j均为酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O据此,下列说法不正确的是( )
2ClO2↑+K2SO4+2CO2↑+2H2O据此,下列说法不正确的是( )
A. KClO3发生还原反应
B. H2C2O4在反应中被氧化
C. H2C2O4的氧化性强于C1O2的氧化性
D. 每1mol C1O2生成,该反应转移的电子数约为6.02×1023
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com