
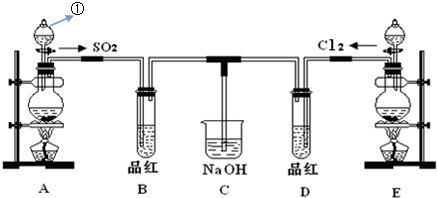
���� װ��A���Ʊ�������������ķ���װ�ã����ɵĶ����������Ư���ԣ�ͨ��װ��B��Ʒ����Һ��ɫ��װ��E���Ʊ������ķ���װ�ã����ɵ�������ˮ��Ӧ�����Ĵ��������ǿ�����ԣ�����Ư���ԣ�ͨ��Ʒ����Һ��ɫ��ʣ����������������װ��C������������Һ���գ���ֹ��Ⱦ������
��1����������������Һ�ķ�Һ©����
��2�����ݻ�ѧ����ʽ��д���ӷ���ʽ�����ݻ��ϼ۵ı仯��ת�Ƶĵ�����Ŀ��������������״���µ������
��3��SO2��Ư���п����ԣ��������Ư�ײ����棻
��4��װ��C�� �������ƿ�������ʣ��Ķ��������������
��5���������н�ǿ�������ԣ�����������н�ǿ�Ļ�ԭ�ԣ���ˮ��Һ�����߷�����ӦCl2+SO2+2H2O�T2HCl+H2SO4��
��� �⣺��1��ʵ������װ��A�Ʊ�SO2�����������ٵ������Ƿ�Һ©����
�ʴ�Ϊ����Һ©����
��2���ڷ�ӦMnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O�У�ÿ��4mol HCl���뷴Ӧ�����������Ȼ�����2mol������1molCl2����ת�����ʵ���2mol����Ӧ�е���0.4mol���ӷ���ת��ʱ��������Cl2�����ʵ���Ϊ0.2mol����״�������=0.2mol��22.4L/mol=4.48L��
�ʴ�Ϊ��4.48��
��3����SO2����Ư���ԣ���������ͨ��Ʒ����Һ�У�Ʒ����ɫ����Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ���ֵ�������Ʒ����Һ��ɫ��
�ʴ�Ϊ��Ʒ����ɫ��Ʒ����ɫ��
��SO2��Ư���п����ԣ���ɫ�����Һ����ʱ�ָֻ�ԭ���ĺ�ɫ��������ˮ��Ӧ���ɵĴ��������Ư���ԣ��������ͨ��Ʒ����Һ��Ҳ��ʹƷ����ɫ���������Ư�ײ����棬����ʱ�����ָܻ���ɫ��
�ʴ�Ϊ����ɫ��Ʒ���ָֻ��ɺ�ɫ������������
��4��װ��C�� �������ƿ�������ʣ��Ķ����������������ֹ��Ⱦ�����ŷţ�
�ʴ�Ϊ����ȥ����Ķ��������������
��5���������н�ǿ�������ԣ�����������н�ǿ�Ļ�ԭ�ԣ���ˮ��Һ������1��1������Ӧ��Cl2+SO2+2H2O�T2HCl+H2SO4�������ﶼ��Ư���ԣ����SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һʱ��Ʒ����Һ������ɫ��
�ʴ�Ϊ��Cl2+SO2+2H2O�T2HCl+H2SO4��
���� ���⿼���������Ͷ��������Ư�����ʣ�ע�����������Ͷ����������ʣ�ע����������Ư������������Ư���Ը���������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1Lˮ���ܽ���58.5g NaCl������Һ�����ʵ���Ũ��Ϊ1mol/L | |
| B�� | V L Fe2��SO4��3��Һ�к�a g SO42-��ȡ����Һ0.5VL��ˮϡ�ͳ�2V L����ϡ�ͺ���Һ��c��Fe3+��Ϊ$\frac{a}{4V}$ mol/L | |
| C�� | ʵ������240mL2mol/L��CuSO4��Һ������ʱӦ��125.0gCuSO4•5H2O | |
| D�� | 10mL��������Ϊ98%��H2SO4����ˮϡ����100mL������������Ϊ9.8% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ӻͼ�ȩ��һ�������¿ɺϳɷ�ȩ��֬ | |
| B�� |  �ĵ����� HOCH2CH2OH �� �ĵ����� HOCH2CH2OH ��  | |
| C�� | �۱���ϩ���ɱ���ϩ�Ӿ����ɵĴ����� | |
| D�� | 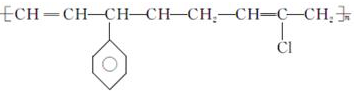 �ĵ�����3�� �ĵ�����3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ��Һ������״̬���ܵ���Ļ������������� | |
| B�� | ��ˮ��Һ������״̬���ܵ���Ļ������������� | |
| C�� | BaSO4������������Ƿǵ���� | |
| D�� | ������ԭ��Ӧ�ı����ǻ��ϼ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ��ʱ��ظ�������Һ�ļ�����ǿ | |
| B�� | ʹ��ʱ������Ag2O�������·����Zn�� | |
| C�� | ��Һ��OH-�������������ƶ� | |
| D�� | Zn�缫������ԭ��Ӧ��Ag2O�缫����������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol Na2O2��ˮ��ȫ��Ӧ��ת�Ƶ�����Ϊ2NA | |
| B�� | 0.5 L 0.2 mol•L-1 FeCl3��Һ�У���Fe3+��Ϊ0.1NA | |
| C�� | ��һ�������£����ֽ�80 g SO3�������������ԭ����Ϊ3NA | |
| D�� | ���³�ѹ�£�28 g��ϩ�ͱ�ϩ������庬�е�̼ԭ������Ϊ2.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
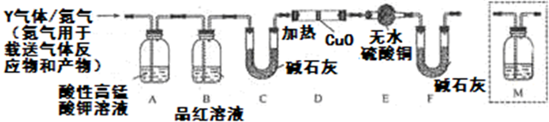
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ���ռ���Һ��ŨH2SO4 | B�� | ����KMnO4��Һ��ŨH2SO4 | ||
| C�� | ����ʯ��ˮ��ŨH2SO4 | D�� | ŨH2SO4������KMnO4��Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com