
| ��ѧʽ | ���볣�� |
| H2SO3 | K1=1.3��10-2��K2=6.2��10-8 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
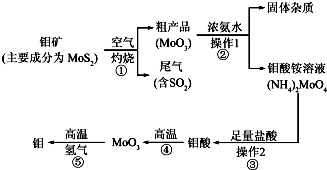
���� �������Ҫ�ɷ���MoS2���ڿ�����ȼ������MoO3��SO2������������������������ܱ���Һ���գ�����β����SO2��Ũ��ˮ���գ�����������л�ԭ�ԣ���ͬʱͨ��������������泥�MoO3��Ũ��ˮ�����������Һ�����˳�ȥ���ʣ����������Һ�м��������ᣬ�������ֽⷴӦ����������Ȼ�泥�����Ϊ������ˮ����Ļ�ɫ���壬���˵õ����ᾧ����·ֽ�����MoO3���ڸ�����������������ԭ�õ������⣮
��1����Ӧ��ΪMoS2������Ӧ����MoO3��SO2������Ԫ���غ���д��ѧ����ʽ��
��2����Ӧ��ΪMoO3��Ũ��ˮ��Ӧ���ɣ�NH4��2MoO4��
��3���������е��볣����֪��HCO3-��H2SO3��Ӧ����H2CO3��HSO3-��HSO3-��CO32-��Ӧ���� HCO3-��SO32-���ݴ��жϣ������̼������Һ��ͨ�������������������������ƺ�̼�����ƣ�
��4���������̷�����֪������1�Ͳ���2��Ϊ���ˣ�������Ҫʹ�õ���Ҫ�����������ձ���©�������������ݴ˴��⣻
��5���������������Ϊ80%��10L����״������Ȼ��������������̼��ˮ�����Ļ�����ڸ����·�Ӧ������ת����Ϊ90%����μӷ�Ӧ�ļ�������ʵ���Ϊ$\frac{10��0.8��0.9}{22.4}$mol=0.32mol�����ݷ���ʽCO2+CH4$\frac{\underline{\;����\;}}{\;}$2CO+2H2��CH4+H2O$\frac{\underline{\;����\;}}{\;}$CO+3H2��֪��ÿĦ������������CO��H2�����ʵ���Ϊ4mol�����ݵ��ӵ�ʧ�غ��֪��ÿĦ��CO��H2���ܲ���$\frac{1}{3}$molMo�������й�ϵʽCH4��$\frac{4}{3}$Mo���ݴ˿ɼ�������������������������
��� �⣺��1����Ӧ��ΪMoS2������Ӧ����MoO3��SO2����Ӧ�Ļ�ѧ����ʽΪ2MoS2+7O2$\frac{\underline{\;����\;}}{\;}$2MoO3+4SO2 ��
�ʴ�Ϊ��2MoS2+7O2$\frac{\underline{\;����\;}}{\;}$2MoO3+4SO2 ��
��2����Ӧ��ΪMoO3��Ũ��ˮ��Ӧ���ɣ�NH4��2MoO4����Ӧ����ʽΪMoO3+2NH3•H2O=��NH4��2MoO4��
�ʴ�Ϊ��MoO3+2NH3•H2O=��NH4��2MoO4��
��3���������е��볣����֪��HCO3-��H2SO3��Ӧ����H2CO3��HSO3-������HCO3-��H2SO3���ܹ��棬HSO3-��CO32-��Ӧ���� HCO3-��SO32-������HSO3-��CO32-���ܹ��棬��ѡCD�������̼������Һ��ͨ�������������������������ƺ�̼�����ƣ���Ӧ�����ӷ���ʽΪ2CO32-+SO2+H2O=SO32-+2HCO3-��
�ʴ�Ϊ��CD��2CO32-+SO2+H2O=SO32-+2HCO3-��
��4���������̷�����֪������1�Ͳ���2��Ϊ���ˣ�������Ҫʹ�õ���Ҫ�����������ձ���©������������
�ʴ�Ϊ���ձ���©������������
��5���������������Ϊ80%��10L����״������Ȼ��������������̼��ˮ�����Ļ�����ڸ����·�Ӧ������ת����Ϊ90%����μӷ�Ӧ�ļ�������ʵ���Ϊ$\frac{10��0.8��0.9}{22.4}$mol=0.321mol�����ݷ���ʽCO2+CH4$\frac{\underline{\;����\;}}{\;}$2CO+2H2��CH4+H2O$\frac{\underline{\;����\;}}{\;}$CO+3H2��֪��ÿĦ������������CO��H2�����ʵ���Ϊ4mol�����ݵ��ӵ�ʧ�غ��֪��ÿĦ��CO��H2���ܲ���$\frac{1}{3}$molMo�������й�ϵʽCH4��$\frac{4}{3}$Mo�������������������������Ϊ0.321mol��$\frac{4}{3}$��96g/mol=41.1g��
�ʴ�Ϊ��41.1��
���� ���⿼�����ʷ�����ᴿ��Ϊ��Ƶ���㣬���ؿ���ѧ������������������ȷÿһ�������ķ�Ӧ�����������ǽⱾ��ؼ����ѵ��ǣ�5������㣬ע������������CO�Լ���֮��Ĺ�ϵ��Ϊ�״��㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶����ߣ�����������ɫ���
���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶����ߣ�����������ɫ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
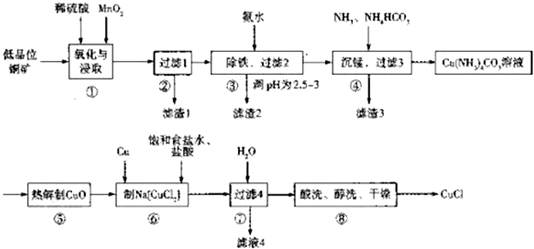
 �����������һ����Ҫ�Ĺ�ҵԭ�ϣ�ij��ѧС�������ͼװ���Ա����ᡢ�״�Ϊԭ����ȡ������������й����ʵ��������ʼ��±���ʾ��
�����������һ����Ҫ�Ĺ�ҵԭ�ϣ�ij��ѧС�������ͼװ���Ա����ᡢ�״�Ϊԭ����ȡ������������й����ʵ��������ʼ��±���ʾ��| ������ | �״� | ��������� | |
| �۵�/�� | 122.4 | -97 | -12.3 |
| �е�/�� | 249 | 64.3 | 199.6 |
| �ܶ�/g��cm-3 | 1.2659 | 0.792 | 1.0888 |
| ˮ���� | �� | ���� | ���� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
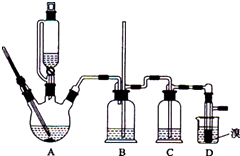 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
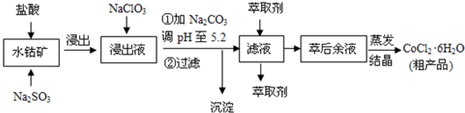
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 |
| ��ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ϩ����ϩ����������ԭ�Ӿ���ͬһƽ�� | |
| B�� | ���͡����͡�ֲ���Ͷ���̼�⻯���� | |
| C�� | 2-������Ҳ���춡�� | |
| D�� | �Ҵ����ױ����屽����ˮ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com