
【题目】反应A(g)+B(g)→C(g)△H,分两步进行:①A(g)+B(g)→X(g)△H1 , ②X(g)→C(g)△H2 , 反应过程中能量变化如图所示,E1表示A(g)+B(g)→X(g)的活化能,下列说法正确的是( ) 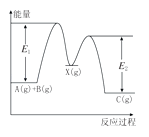
A.△H=E1﹣E2
B.E1是反应①的活化能
C.X是反应A(g)+B(g)→C(g)的催化剂
D.△H2>0
【答案】B
【解析】解:A.①A(g)+B(g)→X(g)△H1 ②X(g)→C(g)△H2 , ①+②得:A(g)+B(g)→C(g)△H=△H1+△H2 , 故A错误;
B.根据图示可知,E1是气体A、B分子从常态转变为容易发生化学反应的活跃状态所需要的能量,为反应①的活化能,故B正确;
若X是反应A(g)+B(g)→C(g)的催化剂,则X是反应①的反应物,是反应②的生成物,故B错误;
C.若X是反应A(g)+B(g)→C(g)的催化剂,则X是反应①的反应物,是反应②的生成物,则X不是反应A(g)+B(g)→C(g)的催化剂,故C错误;
D.根据图示可知,X(g)的总能量大于C(g),则该反应为放热反应,△H2<0,故D错误;
故选B.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将NaC1O3和NaI按物质的量之比1:1混合于烧瓶中,滴入适量硫酸,并水浴加热,反应后测得NaC1O3和NaI恰好完全反应,生成I2、Na2SO4和H2O,并产生棕黄色的气体X,则X为
A. Cl2 B. Cl2O C. Cl2O3 D. ClO2
【答案】D
【解析】试题分析:根据转移电子数守恒得,1molNaI中的碘元素由-1价生成单质碘,化合价升高转移1mol电子,故NaClO3中的氯元素化合价降低转移1mol电子,故X气体中氯元素的价态为+4价,答案选D.
考点:氧化还原反应
【题型】单选题
【结束】
25
【题目】把4.48LCO2通过一定量的固体过氧化钠后收集到3.36L气体(气体的测量均在标准状况下),所得气体的总质量是
A. 3.2g B. 4.8g C. 5.4g D. 6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制取氨气并完成喷泉实验(图中夹持装置均已略去). 
(1)写出实验室制取氨气的化学方程式 .
(2)收集氨气应使用法,要得到干燥的氨气可选用作干燥剂.
(3)用图Ⅰ所示装置进行喷泉实验,上部烧瓶已装满干燥的氨气,引发喷泉的操作是 , 该实验的原理是 .
(4)如果只提供如图Ⅱ所示装置,请说明引发喷泉的方法是
(5)写出氨气催化氧化的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就三大酸与金属反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解.该反应的化学方程式为: .
(2)在一定体积的10molL﹣1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol.则浓硫酸的实际体积(填“大于”、“等于”或“小于”)180mL.若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为 .
(3)欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是
A.浓盐酸
B.稀硝酸
C.冷的浓硝酸
D.冷的浓硫酸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将25℃、101kPa 条件下的氯化氢(HCl)气体49.6 L,通入127 mL 水中( 已知水的密度为1.00g·cm-3),得到密度为1.19g.cm-3的盐酸。(已知:25℃、101kPa条件下,气体摩尔体积为24.8 L·mol -1)
(1)此盐酸中溶质的质量分数是多少?________________
(2)此盐酸中HCl 的物质的量浓度是多少?_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一恒温恒容密闭容器中充入1mol CO2和3mol H2 , 一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol
测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.下列说法正确的是( )
A.反应进行到3 min时,该反应达到平衡状态
B.从反应开始到平衡,CO2的转化率为25%
C.第3 min时,氢气的平均反应速率为1.5mol/(L?min)
D.该温度下,反应的平衡常数的值为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确认HCl、H2CO3、H2SiO3的酸性强弱,某学生设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。请据此回答:
①锥形瓶中装某可溶性正盐溶液,分液漏斗所盛试剂应为。
②装置B所盛的试剂是 , 其作用是。
③装置C所盛试剂是 ,
C中反应的离子方程式是。
④由此可得出的结论是:酸性>>。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.若烃中碳、氢元素的质量分数相同,则为同系物
B.CH2═CH2和CH2═CH﹣CH═CH2互为同系物
C.![]() 和
和 ![]() 互为同分异构体
互为同分异构体
D.同分异构体的化学性质可能相似
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com