
【题目】下列有关物质分类正确的是
①混合物:盐酸、王水、水玻璃、水银
②化合物:CaCl2、烧碱、聚苯乙烯、HD
③电解质:H2SO4、胆矾、冰醋酸、硫酸钡
④同素异形体:C60、C70、金刚石、石墨.
A. ①③ B. ②④ C. ②③ D. ③④
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 浓度均为0.1000mol/L 的三种酸HX、HY、HZ,滴定曲线如图所示。下列说法不正确的是
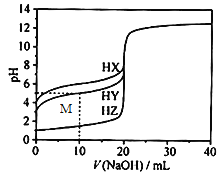
A. 该滴定过程能选择酚酞作为指示剂
B. HZ是强酸
C. HX消耗NaOH溶液20.00mL时,溶液pH>7
D. M 点处的溶液中c(Na+)>c(Y-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化如图所示.下列因素中,影响反应速率的因素是( )
①盐酸的浓度 ②镁条的表面积 ③溶液的温度④Cl﹣的浓度.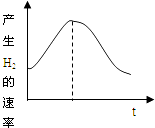
A.①④
B.③④
C.①②③
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有以下几种措施:①对燃烧煤时产生的尾气进行脱硫处理②少用原煤做燃料③燃煤时鼓入足量空气④开发清洁能源。其中能减少酸雨产生的措施是
A. ①②③ B. ②③④
C. ①②④ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4是天然气的主要成分,而液化石油气的主要成分是丙烷、丁烷、丙烯(C3H6)、丁烯(C4H8).下列说法中不正确的是( )
A.相同物质的量上述5种烃中,消耗O2体积最大的是丁烷
B.相同质量上述5种烃中,生成H2O的质量最大的是CH4
C.天然气灶具改用液化石油气时,应将进风口改小
D.严冬季节液化石油气有时会出现火焰变小的现象原因是有些成分被液化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂
B.SiO2有导电性,可用于制备光导纤维
C.明矾能水解生成Al(OH)3胶体,可用作净水剂
D.Al2O3熔点高,可用于制作耐高温仪器
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出). 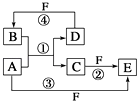
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,反应①的化学方程式Na2CO3:0.1mol;NaHCO3:0.05mol.
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,且光照条件下D与F也可以反应,则反应②的离子方程式是Na2CO3:0.1mol;NaHCO3:0.05mol.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为Na2CO3:0.1mol;NaHCO3:0.05mol.将标准状况下3.36L 物质E 与含10.0g 氢氧化钠溶质的溶液充分反应,所得溶液溶质成分为Na2CO3:0.1mol;NaHCO3:0.05mol(写出化学式和对应的物质的量).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一体积为10 L的密闭容器中,通入一定量的CO和H2O,在850 ℃时发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。CO和H2O浓度变化如图所示,则0~4 min的平均反应速率v(CO)=_____________ mol/(L·min)。
CO2(g)+H2(g) ΔH<0。CO和H2O浓度变化如图所示,则0~4 min的平均反应速率v(CO)=_____________ mol/(L·min)。

(2)t℃(高于850 ℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如表:
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c3 |
4 | c1 | c2 | c3 | c3 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
①表中3~4 min时,反应处于_______________状态;c1数值_____________0.08 mol/L(填“大于”、“小于”或“等于”)。
②反应在4~5 min时,平衡向逆方向移动,可能的原因是____________(填字母,下同),表中5~6 min时,数值发生变化,可能的原因是________________。
a.增加水蒸气b.降低温度
c.使用催化剂d.增加氢气浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com