
【题目】氯气是一种重要的化工原料。氯化氢催化氧化制氯气的化学方程式为4HCl+O2![]() 2Cl2+2H2O。该反应中,作为氧化剂的物质是___________,被氧化的物质是____________,若反应中消耗了4 mol HCl,则生成________mol Cl2。
2Cl2+2H2O。该反应中,作为氧化剂的物质是___________,被氧化的物质是____________,若反应中消耗了4 mol HCl,则生成________mol Cl2。
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A (g)+B(g)2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(Lmin),下列说法错误的是( )
A.x=2
B.B的转化率为20%
C.平衡时A的浓度为0.75mol/L
D.恒温达平衡时容器内的压强为开始时的85%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X元素的阳离子与Y的阴离子具有相同的核外电子排布,则下列比较中正确的是( )
A.原子序数: X<YB.原子半径:X<Y
C.离子半径:X<Y D.原子最外层电子数:X<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)紫薯营养丰富,具有特殊的保健功能。下表是100 g紫薯粉的营养成分含量表:
营养成分 | 含量(每100 g) | 营养成分 | 含量(每100 g) |
水分 | 9.9 g | 钙元素 | 23.00 mg |
脂肪 | 0.2 g | 铁元素 | 1.10 mg |
蛋白质 | 4.8 g | 硒元素 | 0.02 mg |
淀粉 | 82.5 g | 花青素 | 0.10 g |
纤维素 | 2.7 g | 其他 | …… |
①以上营养成分中,______是人体中含有的微量元素。
②紫薯粉中的脂肪在人体内会水解成高级脂肪酸和______。
③蛋白质在人体内水解的最终产物是氨基酸,其结构可表示为R—CH(NH2)—X,则“—X”的名称为___。
④在酶的作用下,淀粉水解为葡萄糖,葡萄糖再转化为乙醇和二氧化碳。写出葡萄糖转化为乙醇的化学方程式______。
(2)合理饮食、正确使用药物对人体健康至关重要。
①“中国居民平衡膳食宝塔”如图所示,位于最上层且每天不超过25g的能量物质是______。
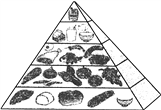
②某品牌饼干的配料标签如图所示,其中苯甲酸钠的作用是______。

③三硅酸镁(Mg2Si3O8·nH2O)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O等物质的化学方程式______。
(3)材料的生产与使用是人类文明和生活进步的一个重要标志。
①我国C919大型客机的机身蒙皮使用的是第三代铝锂合金材料,选用铝锂合金的优点是______(任答一点)。
②铁路建设中如何防止铁轨的腐蚀是工程技术人员攻克的难题之一。钢铁在潮湿的空气中易发生吸氧腐蚀如图所示,则正极的电极反应式为______。
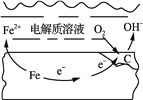
③玻璃中加入适量的溴化银(AgBr)和氧化铜的微小晶粒,经过适当的热处理,可以制成变色玻璃,请写出强光照射变色玻璃时发生反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知空气—锌电池的电极反应为锌片:Zn+2OH--2e-=ZnO+H2O;碳棒:O2+2H2O+4e-=4OH-,据此判断,锌片是( )
A.正极,被还原B.正极,被氧化
C.负极,被还原D.负极,被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素摄入不当也会导致代谢疾病,下列做法的主要目的与补充微量元素有关的是( )
A.咖啡加糖
B.炒菜加味精
C.酱油加铁强化剂
D.加工食品加防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下图所示实验装置的K闭合,下列判断正确的是
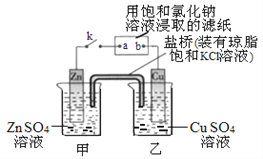
A. Zn电极上发生还原反应
B. 片刻后盐桥中的Cl-向乙装置中移动
C. 当电路中有0.2mol电子转移时,甲池增重质量为6.5克
D. 电子的流动方向从Zn→a ; b→Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两等份。向其中一份中逐渐加入铜粉,最多能溶解19.2g (已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是

A. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
B. 原混合酸中SO42-物质的量为0.6 mol
C. 第二份溶液中最终溶质为FeSO4
D. 取20mL原混合酸加水稀释至1L后溶液的c(H+)=0.2mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com