

 ��
�� ������K�Ľṹ��ʽ
������K�Ľṹ��ʽ ��
��

���� �������и�����ת����ϵ��G��������A��A����������Ӧ��C��C�ữ��E��G��E����������Ӧ��H������H�ķ���ʽ��֪GΪ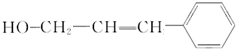 ��AΪ
��AΪ ��CΪ
��CΪ ��EΪ
��EΪ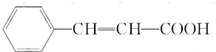 ��HΪ
��HΪ ��A�������ӳɵ�BΪ
��A�������ӳɵ�BΪ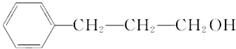 ��E���巢���ӳɷ�Ӧ��DΪ
��E���巢���ӳɷ�Ӧ��DΪ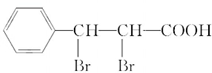 ��D������ȥ��Ӧ��IΪ
��D������ȥ��Ӧ��IΪ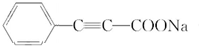 ��I�ữ��JΪ
��I�ữ��JΪ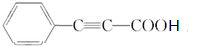 ��E�������ӳɵ�FΪ
��E�������ӳɵ�FΪ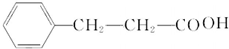 ��E�����Ӿ۷�Ӧ��KΪ
��E�����Ӿ۷�Ӧ��KΪ ���ݴ˴��⣮
���ݴ˴��⣮
��� �⣺�������и�����ת����ϵ��G��������A��A����������Ӧ��C��C�ữ��E��G��E����������Ӧ��H������H�ķ���ʽ��֪GΪ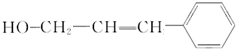 ��AΪ
��AΪ ��CΪ
��CΪ ��EΪ
��EΪ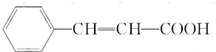 ��HΪ
��HΪ ��A�������ӳɵ�BΪ
��A�������ӳɵ�BΪ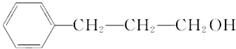 ��E���巢���ӳɷ�Ӧ��DΪ
��E���巢���ӳɷ�Ӧ��DΪ ��D������ȥ��Ӧ��IΪ
��D������ȥ��Ӧ��IΪ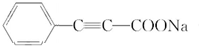 ��I�ữ��JΪ
��I�ữ��JΪ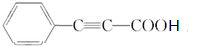 ��E�������ӳɵ�FΪ
��E�������ӳɵ�FΪ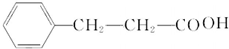 ��E�����Ӿ۷�Ӧ��KΪ
��E�����Ӿ۷�Ӧ��KΪ ��
��
��1��AΪ ��A��������������̼̼˫�������Ľṹʽ��
��A��������������̼̼˫�������Ľṹʽ�� ��
��
�ʴ�Ϊ�� ��
��
��2����������ķ�����֪����ͼ��ʾ��ת����ϵ �١����У��л����������Ӧ���Ǣ٢ڣ�
�ʴ�Ϊ���٢ڣ�
��3������C�Ľṹ��ʽ�� ������K�Ľṹ��ʽ��
������K�Ľṹ��ʽ�� ��
��
�ʴ�Ϊ�� ��
�� ��
��
��4����Ӧ�۵Ļ�ѧ����ʽΪ ��
��
��Ӧ��Ļ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��5��FΪ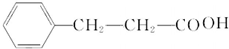 �����б������ұ�����ֻ��һ����������������F��ͬ���칹��Ϊ��������-CH2COOCH3��-COOCH2CH3��HCOOCH2CH2-��HCOOCH��CH3��-��CH3COOCH2-��CH3CH2COO-����6�֣�
�����б������ұ�����ֻ��һ����������������F��ͬ���칹��Ϊ��������-CH2COOCH3��-COOCH2CH3��HCOOCH2CH2-��HCOOCH��CH3��-��CH3COOCH2-��CH3CH2COO-����6�֣�
�ʴ�Ϊ��6��
���� ���⿼���л�����ƶϣ��ѶȺܴ�Ϊ�״���Ŀ������A�����ķ�Ӧ���������ʽȷ�����еĹ�������Ŀ��̼ԭ����Ŀ�ǹؼ����ٽ��ת����ϵ��H�ķ��ӽ�������G��E�к��еĹ����ţ������ѧ�����������кܸߵ�Ҫ��


 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
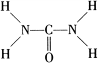 ���������ؿ��������л����ʣ���Ҫ�������������������غ���������ѧʽΪ[Fe��H2NCONH2��6]��NO3��3����ش��������⣺
���������ؿ��������л����ʣ���Ҫ�������������������غ���������ѧʽΪ[Fe��H2NCONH2��6]��NO3��3����ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | Sr��OH��2��Һ�����/mL | ��������/mL | ��Һ��pH |
| �� | |||
| �� | 22.00 | 18.00 | 7 |
| �� | 22.00 | 22.00 | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ����̿��mol�� | NO��mol�� | CO2��mol�� | N2��mol�� | |
| ��ʼ״̬ | 3.0 | 0.8 | 0 | 0 |
| 2minʱ | 2.8 | 0.4 | 0.2 | 0.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������� | B�� | ���� | C�� | �Ҵ� | D�� | ��ȩ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij�����A������Al2��SO4��3��Al2O3��Fe2O3����һ���������¿�ʵ����ͼ��ʾ�ı仯����ش��������⣺
ij�����A������Al2��SO4��3��Al2O3��Fe2O3����һ���������¿�ʵ����ͼ��ʾ�ı仯����ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ�е������ӵ���Ŀ���� | |
| B�� | ��ֵ$\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$���� | |
| C�� | ����ĵ���̶�����c��H+�������� | |
| D�� | �ټ���10mL pH=11��NaOH��Һ�����ҺpH=7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɢ������ֱ������10-9 m��10-7m֮��ķ�ɢϵ��Ϊ���� | |
| B�� | ��Ӿ�����֤��������е�� | |
| C�� | �þ۹��ֵ�Ͳ����FeCl3��Һ��Fe��OH��3����ʱ��������������ͬ | |
| D�� | Fe��OH��3������ˮ����˿���������е�����������Һ�еμӱ������Ȼ�����Һ�ķ����Ʊ������������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com