
����Ŀ��̼Ԫ�����γɶ��ֵ�������ʯ��ʯī�ȣ�24g ���ʯ�к���_______��̼̼������̼Ԫ��Ҳ���γɶ��ֻ�������γɻ�����ʱ�������ɻ�ѧ���Թ��ۼ�Ϊ����ԭ���� _______��
(1)��ҵ��þʱ����� MgCl2 ������� MgO ��ԭ���� _______��
(2)BeCl2 �۵�ϵͣ����������������л��ܼ����ɴ˿��Ʋ� BeCl2 ����Ϊ _______���壨������ͣ��������Ϊ_______���ӣ����������������Ǽ������������ӹ���Ϊ_______��BeCl2 �۵�_______��ѡ����������������������BeBr2��
���𰸡�4NA C �� 4 ���۵����Ұ뾶��С������ͨ���û�ʧ���Ӵﵽ�ȶ��ṹ MgCl2 �� MgO ��Ϊ���Ӿ��壬Cl-�뾶���� O2-�뾶����� MgO ���������Ӽ����ܴ��� MgCl2���۵�ϸߣ�����ʱ���ĸ������������������ɱ� ���� �Ǽ��� ֱ���� ����
��������
���ʯ�ĽṹƬ��Ϊ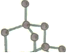 ���Ӵ˽ṹƬ���п��Կ�����ÿ��Cԭ������Χ��4��Cԭ���γɹ��۵�����ÿ�����۵����������ڵ�2��Cԭ�ӣ����ԣ�ƽ��ÿ��Cԭ���γɹ��ۼ�����ĿΪ4��
���Ӵ˽ṹƬ���п��Կ�����ÿ��Cԭ������Χ��4��Cԭ���γɹ��۵�����ÿ�����۵����������ڵ�2��Cԭ�ӣ����ԣ�ƽ��ÿ��Cԭ���γɹ��ۼ�����ĿΪ4��![]() =2��
=2��
�����Ϸ�����֪���ڽ��ʯ�����У�ƽ��ÿ��Cԭ���γ�2�����ۼ���24g ���ʯ�к���![]() =4NA��̼̼������̼Ԫ�ص�����������Ϊ4����ʧ���Ӷ����ѣ����γɻ�����ʱ�����γɻ�ѧ���Թ��ۼ�Ϊ����ԭ����C �� 4 ���۵����Ұ뾶��С������ͨ���û�ʧ���Ӵﵽ�ȶ��ṹ����Ϊ��4NA��C �� 4 ���۵����Ұ뾶��С������ͨ���û�ʧ���Ӵﵽ�ȶ��ṹ��
=4NA��̼̼������̼Ԫ�ص�����������Ϊ4����ʧ���Ӷ����ѣ����γɻ�����ʱ�����γɻ�ѧ���Թ��ۼ�Ϊ����ԭ����C �� 4 ���۵����Ұ뾶��С������ͨ���û�ʧ���Ӵﵽ�ȶ��ṹ����Ϊ��4NA��C �� 4 ���۵����Ұ뾶��С������ͨ���û�ʧ���Ӵﵽ�ȶ��ṹ��
(1)��ҵ��þʱ��MgCl2��MgO��Ϊ���ӻ��������ʱ���ܵ��磬���۵������ܲ����� MgCl2 ������� MgO ��ԭ����MgCl2 �� MgO ��Ϊ���Ӿ��壬Cl-�뾶���� O2-�뾶����� MgO ���������Ӽ����ܴ��� MgCl2���۵�ϸߣ�����ʱ���ĸ������������������ɱ�����Ϊ��MgCl2 �� MgO ��Ϊ���Ӿ��壬Cl-�뾶���� O2-�뾶����� MgO ���������Ӽ����ܴ��� MgCl2���۵�ϸߣ�����ʱ���ĸ������������������ɱ���
(2)BeCl2 �۵�ϵͣ����������������л��ܼ������Ϸ��Ӿ�������ʡ��ɴ˿��Ʋ� BeCl2 ����Ϊ���Ӿ��壬Be����������ȫ�����ڳɼ��������Ϊ�Ǽ��Է��ӣ����ӹ���Ϊֱ���ͣ����Ӿ�����۵�����Է��������йأ�ͨ����Է�������Խ���Ӽ�������Խ���۵�Խ�ߣ�BeCl2 �۵����BeBr2����Ϊ�����ӣ��Ǽ��ԣ�ֱ���ͣ����ڡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У�����֤����Ӧ N2��3H2![]() 2NH3 �Ѵ�ƽ��״̬���ǣ� ��
2NH3 �Ѵ�ƽ��״̬���ǣ� ��
A. һ��N��N�����ѵ�ͬʱ��������H��H���γ�
B. һ��N��N�����ѵ�ͬʱ��������H��H������
C. һ��N��N�����ѵ�ͬʱ��������N��H������
D. һ��N��N�����ѵ�ͬʱ��������N��H���γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����SO2ͨ������Fe2(SO4)3��Һ��,��ȫ��Ӧ���ټ���K2CrO4��Һ,������������ѧ��ӦΪSO2+2Fe3++2H2O=SO42-+2Fe2++W����,Cr2O72-+aFe2++bH+![]() Cr3++Fe3++H2O����,�����й�˵����ȷ����
Cr3++Fe3++H2O����,�����й�˵����ȷ����
A. ��ԭ��:Cr3+>SO2 B. ��ƽ��ʽ����,a=6,b=7
C. Cr2O72-�ܽ�Na2SO3������Na2SO4 D. ����ʽ����WΪOH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ������������Ȼ����ˮ������Ӧ�Ʊ�������Ҫ��ӦΪ��
CH4+ 2H2O![]() CO2+4H2����֪��
CO2+4H2����֪��
CH4��g��+2O2��g����CO2��g��+2H2O��l�� ��H=-890kJ/mol
2H2��g��+O2��g����2H2O��l�� ��H=-571.6kJ/mol
H2O��g����H2O��l�� ��H=-44kJ/mol
��1��д������Ȼ����ˮ������Ӧ�Ʊ�H2���Ȼ�ѧ����ʽ��____________��
��2��ij�¶��£�10L�ܱ������г���2mol CH4��3mol H2O��g��������CH4��g��+ 2H2O��g��![]() CO2��g��+4H2��g����Ӧ����һ��ʱ�䷴Ӧ��ƽ�⣬ƽ��ʱ������ѹǿ����ʼʱ��1.4����
CO2��g��+4H2��g����Ӧ����һ��ʱ�䷴Ӧ��ƽ�⣬ƽ��ʱ������ѹǿ����ʼʱ��1.4����
����ƽ��ʱ��CH4��ת����Ϊ__________��H2��Ũ��Ϊ_________����Ӧ���ų�����������_______kJ��
������ƽ����ϵ���¶�,��������ƽ����Է�������___________,�ܶ�_________�����������������С����������������
�����ﵽƽ��ʱ,�������,������ѹǿ����,ƽ�⽫___________�������������������������������ƶ���
�������ֺ��£�������ѹ��Ϊ5L���������Ծ�Ϊ��̬����ƽ�⽫________�������������������������������ƶ����ﵽ��ƽ���,������H2Ũ�ȷ�ΧΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��50 mL 0.50 mol��L1������50 mL 0.55 mol��L1 NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
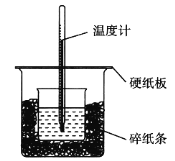
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��______________________________��
��2���ձ���������ֽ����������______________��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ__________(����ƫ������ƫС��������Ӱ����)��
��4��ʵ���и���60 mL 0.50 mol��L1�����50 mL 0.55 mol��L1 NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������__________(��������������������)�������к���__________(��������������������)���������ɣ�_________________________��
��5������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��__________(����ƫ������ƫС��������Ӱ��������ͬ)����50 mL 0.50 mol��L1 NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�������ﵽʵ��Ŀ�ĵ���( )
A. ʵ������ȡ����
ʵ������ȡ����
B.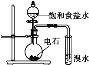 ֤����Ȳ��ʹ��ˮ��ɫ
֤����Ȳ��ʹ��ˮ��ɫ
C.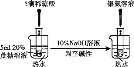 �������ǵ�ˮ�������л�ԭ��
�������ǵ�ˮ�������л�ԭ��
D.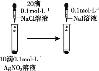 ֤���ܽ�ȣ�AgCl��AgI
֤���ܽ�ȣ�AgCl��AgI
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25�棬��0.10mol/LNaOH��Һ�ζ�20.00mL������Һ��20.00mL���ᣬ�ζ�������ͼ��ʾ������˵������ȷ����
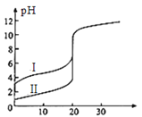
A.���ߢ�ֱ��ʾ������Һ������ĵζ�����
B.�ﵽ�ζ��յ�ʱ������ҺpH������7
C.��ʼʱ�����Ũ��Ϊ0.10mol/L
D.�ζ�������Һ������ʱ������ѡ���̪��Һ��ָʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�鼰�������Ƴ���Ӧ���۵���
ʵ�������ʵ������ | �� �� | |
A | ��2mL 0.5mol/L FeCl3��Һ�еμ�2mL 1mol/L KSCN��Һ�����ã��۲쵽��Һ��ɺ�ɫ������1mL 2mol/L KCl��Һ����Һ��ɫ��dz | c(KCl)����ʹ�÷�Ӧ[FeCl3+ 3KSCN |
B | ��������ͬ��ǵ�2֧�Թ��о�����2mL 0.1mol/L Na2S2O3��Һ���ٷֱ���2֧�Թ��м���4mLŨ��Ϊ0.1mol/L��0.5mol/L ��H2SO4��Һ���ⶨǡ���ڵ�ȫ���������ʱ�� | ��������һ��ʱ����Ӧ��Ũ��Խ��ѧ��Ӧ����Խ�� |
C | �����£��ù㷺pH��ֽ�ⶨ0.1 mol/L Na2SO3��Һ��pHΪ10��0.1mol/L NaHSO3��Һ��pHΪ5 | ��ͬ�����£�HSO3����ˮ������ǿ��SO32�� |
D | ��2 mL0.1mol/LAgNO3��Һ�м���1mL0.1mol/LNaCl��Һ�����ɰ�ɫ�������ټ���1mL0.1mol/L KI��Һ�����ɻ�ɫ���� | Ksp(AgI)��Ksp(AgCl) |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨ���ᾧ��H2C2O4��xH2O�е�xֵ��ijʵ��С�����ʵ�飬�������£�
�ٳ�ȡ1.260g���ᾧ�壬���100mL��Һ��
��ȡ25.00mL��H2C2O4��Һ������ƿ�ڣ��ټ�������ϡ���ᡣ
����Ũ��Ϊ0.1000mol/L��KMnO4��Һ�ζ�H2C2O4��Һ����_________________ʱ���ζ�������
�ܼ�¼���ݣ��ظ�ʵ�顣�����������£�
ʵ����� | V(KMnO4��Һ) | |
�ζ�ǰ�̶�/mL | �ζ���̶�/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
�ش��������⣺
(1)�������Ҫʹ���ձ�����Ͳ������������ȱ�ٵIJ�������Ϊ_______(������)������۵ζ������У�ʢװKMnO4��Һ������Ϊ______(������)��
(2)�÷�Ӧԭ���Ļ�ѧ����ʽΪ_________________��
(3)�뽫����۲�������__________________��
(4)�������ݣ�����H2C2O4��Һ�����ʵ���Ũ��Ϊ______________mol/L��x=____________��
(5)���ζ��յ����ʱ����KMnO4��ҺҺ�棬��xֵ��__________(����ƫ��������ƫС��������Ӱ����)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com