
| A. | NaCl的摩尔质量是58.5g | |
| B. | 0.5 mol CO2 中所含的CO2 分子数为 3.01×1023 | |
| C. | 标准状况下,6.02×1022 个CO2 所占的体积约是 22.4 升 | |
| D. | 在 l L 水中溶解5.85g NaCl固体,即可配制得0.1 mo1/L 的NaCl溶液 |
分析 A.摩尔质量的单位为g/mol;
B.结合N=nNA计算;
C.结合N=nNA、V=nVm计算;
D.l L 水为溶剂的体积,不是溶液的体积.
解答 解:A.NaCl的摩尔质量是58.5g/mol,故A错误;
B.0.5 mol CO2 中所含的CO2 分子数为0.5NA=3.01×1023,故B正确;
C.标准状况下,6.02×1022 个CO2 所占的体积约是$\frac{6.02×1{0}^{22}}{6.02×1{0}^{23}}$×22.4L/mol=2.24 升,故C错误;
D.l L 水为溶剂的体积,不是溶液的体积,不能计算浓度,故D错误;
故选B.
点评 本题考查物质的量的计算,为高频考点,把握质量、物质的量、体积及微粒数的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 Na2CO3溶液中CO32-、HCO3-和H2CO3总数为0.1 NA | |
| B. | NaCl的沸点为1465℃,1500℃时气体摩尔体积是Vm,此状态下,3Vm L的氯化钠含有3 NA个共价键 | |
| C. | 25℃,1 L pH=1的稀硫酸中含有的H+数为0.1 NA | |
| D. | 1 mol Cu和足量稀硝酸反应产生$\frac{2}{3}$ NA个NO分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
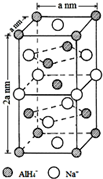 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. .
.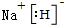 .
.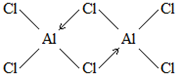 (标明配位键).
(标明配位键).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极发生的反应为:Fe-2e-═Fe2+ | |
| B. | 正极发生的反应为:2H2O+O2+2e-═4OH- | |
| C. | 钢和铁都是铁合金,所以它们的组成基本相同 | |
| D. | 插在水中的钢柱在水下部分比在空气与水交界处更容易腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 主要仪器 | 试剂 |
| A | 配制480mL 2mol/L的NaOH溶液 | 胶头滴管、烧杯、玻璃棒、托盘天平、480mL容量瓶 | NaOH固体、蒸馏水 |
| B | 分离I2和CCl4的混合物 | 分液漏斗、烧杯 | 乙醇 |
| C | 鉴别Na2CO3和NaHCO3溶液 | 试管、胶头滴管 | 澄清石灰水 |
| D | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
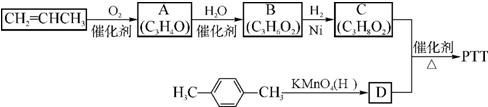
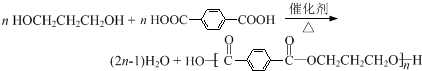 ,反应类型为缩聚反应.
,反应类型为缩聚反应. (须注明反应条件).
(须注明反应条件).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | 只有④ | D. | 全部不是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com