
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源:2014届江苏省泰州市姜堰区高三上学期期中考试化学试卷(解析版) 题型:实验题
镁在高温下与O2、N2或CO2均可以发生反应,试解决下列问题。
(1)工业通常采用电解熔融氯化镁冶炼金属镁,不以氧化镁为原料的理由是 。
(2)将燃着的镁条伸入盛满CO2的集气瓶中,镁条剧烈燃烧,发出耀眼的白光,瓶内壁上有黑色物质生成,化学方程式为 。
(3)由金红石(TiO2)制取单质钛(Ti),涉及到的反应步骤为
金属镁的作用为 ,在Ar气氛中的进行的理由是 。
(4)现拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。已知:
Mg+H2O MgO+H2↑ Mg3N2
+6H2O = 3Mg(OH)2+2NH3↑
MgO+H2↑ Mg3N2
+6H2O = 3Mg(OH)2+2NH3↑
可供选择的装置和药品如下图所示。

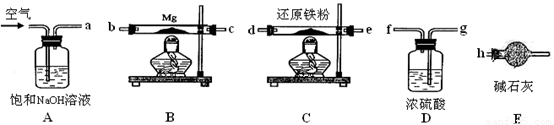
①导管口间的连接次序是:a →( )()→()()→()()→ h
②通气后,应先点燃 (填“B”或“C”)装置的酒精灯,装置A的作用是 ,装置E的作用是 。
③请设计一个简单的小实验验证产物是氮化镁 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com