
(14分)A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化关系如图所示(部分产物已略去)。
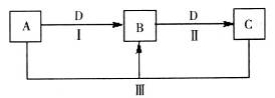
请按要求回答下列问题:
(1)若B、D为短周期同一主族的非金属单质,则反应(III)中氧化产物与还原产物的物质的量之比为___。
(2)若A、B、C均为短周期元素组成的化合物,且溶液都显碱性,D为植物光合作用必须吸收的气体,物质A中化学键的类型为______________________,相同温度下的溶解度B____________C(填“大于、小于、等于”)。
(3)若D为某金属单质,向C的溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则检验B溶液中阳离子的试剂为_________;C的溶液保存时,常加入D的目的是__________________。
(4)若D为强电解质溶液,A和C在溶液中反应生成白色沉淀B,写出反应(III)的离子方程式是_______________________________;符合条件的D物质可能是_______________(填序号)。
①硫酸 ②碳酸 ③氢氧化钠 ④一水合氨 ⑤氯化钡
(1)2:1 (2)离子键和共价键(或离子键和极性键);大于
(3)硫氰化钾溶液;防止溶液里的Fe2+被氧化 (4)Al3++3Al[(OH)3]4-=4Al(OH)3↓;①③
【解析】
试题分析:(1)若B、D为短周期同一主族的非金属单质,则A是H2S,B是S,D是氧气,C是SO2,反应(III)的方程式为2H2S+SO2=3S+2H2O,其中H2S 是还原剂,SO2是氧化剂,因此氧化产物与还原产物的物质的量之比为2:1;
(2)若A、B、C均为短周期元素组成的化合物,且溶液都显碱性,D为植物光合作用必须吸收的气体,则D是CO2,所以A是氢氧化钠,B是碳酸钠,C是碳酸氢钠,氢氧化钠中化学键的类型为离子键和极性键;在相同温度下碳酸钠的溶解度大于碳酸氢钠的溶解度。
(3)若D为某金属单质,向C的溶液中滴加硝酸银溶液,产生不溶于稀硝酸的白色沉淀,则C中含有氯离子,所以A是氯气,B是氯化铁,C是氯化亚铁。检验B溶液中铁离子的试剂为KSCN溶液;亚铁离子易被氧化为铁离子,因此氯化亚铁的溶液保存时,常加入铁的目的是防止溶液里的Fe2+被氧化。
(4)若D为强电解质溶液,A和C在溶液中反应生成白色沉淀B,如果D是强碱,则A是铝盐,B是氢氧化铝,C是偏铝酸盐。如果D是强酸,则A是偏铝酸盐,B是氢氧化铝,C是铝盐,因此反应(III)的离子方程式是Al3++3Al[(OH)3]4-=4Al(OH)3↓,所以符合条件的D物质可能是硫酸或氢氧化钠,碳酸、一水合氨均是弱电解质,氯化钡不反应,答案选①、③。
考点:考查无机框图题的推断


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:2015届山东省菏泽市高三上学期期中联考化学试卷(A)(解析版) 题型:填空题
(11分)A+B→X+Y+ H2O(为配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1∶4.请回答:
(1)若Y是黄绿色气体,则Y的电子式是 ,该反应的化学方程式是 .
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 .
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中.
①A元素在周期表中的位置是______(填所在周期和族);Y的化学式是______.
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是______ mol.
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:实验题
(10分)某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:
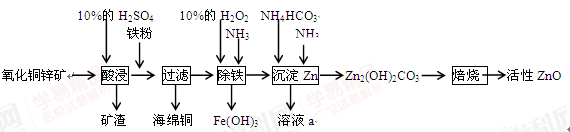
请回答下列问题:
(1)加入铁粉后发生反应的离子方程式为_________________________,_______ _。
(2)甲、乙两同学选用下列仪器,采用不同的方法制取氨气。
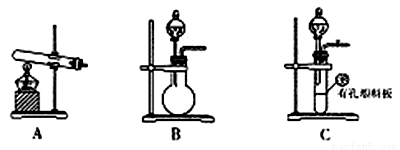
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置_______(填写装置代号),生成氨气的化学方程式为_______________________________________;
②乙同学选用了装置B,则使用的两种药品的名称为______________ _。
(3)H2O2的作用是____________________________________________________。
(4)除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
(5)已知溶液a中含有CO2- 3、SO2- 4两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为_____________________________
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
若NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.常温下,7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.1NA
B.标准状况下,11.2LNH3所含共价键的数为3NA
C.标况下11.2LNO和11.2LO2混合后所得气体分子数为NA
D.2Llmol/L的醋酸溶液中所含氢离子数为2NA
查看答案和解析>>
科目:高中化学 来源:2015届山东省聊城市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列有关原子结构、元素性质的说法正确的是( )
A.ⅠA族元素的金属性一定比ⅡA族的金属性强
B.族序数等于周期序数的元素一定是金属元素
C.全部由非金属元素组成的化合物中只含共价键
D.13C和14C互为同位素,化学性质相似
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:选择题
在铝制易拉罐中收集一满罐CO2,加入过量浓NaOH溶液,立即把口封闭。发现易拉罐“咔咔”作响,并变瘪了;过一会儿后,易拉罐又会作响并鼓起来。则下列说法错误的是
A.导致易拉罐变瘪的反应是:CO2+2OH-=CO32-+H2O
B.导致易拉罐又鼓起来的反应是:2A1+2OH-+6H2O=2 Al[(OH)4]-+3H2↑
C.取易拉罐内反应后的溶液,逐滴加入足量的盐酸,只能发生3个化学反应
D.如果将CO2换为NH3,浓NaOH溶液换为浓盐酸,易拉罐也会出现先瘪后鼓的现象
查看答案和解析>>
科目:高中化学 来源:2015届山东省烟台市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
B.能使润湿的淀粉KI试纸变成蓝色的物质一定是C12
C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I-
D.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
查看答案和解析>>
科目:高中化学 来源:2015届山东省潍坊市高三上学期期中考试化学试卷(解析版) 题型:选择题
中学常见物质A、B、C、D存在下图转化关系(部分生成物和反应条件略去)。该转化关系中A可能是下列物质中的
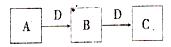
①金属钠 ②硫单质 ③NH3 ④Na2CO3 ⑤AlCl3溶液 ⑥单质铁
A.3 B.4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三10月阶段性考试化学试卷(解析版) 题型:选择题
下列化学反应的离子方程式正确的是( )
A.氢氧化镁中滴加盐酸:H++OH-=H2O
B.用FeCl3溶液腐蚀铜电路板:Fe3++Cu=Fe2++Cu2+
C.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.NH4HCO3溶液中加入过量NaOH溶液并加热:
NH4++HCO3-+2OH-△NH3?+CO32-+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com