
2013ФъГѕ,ЮэіВЬьЦјЖрДЮЫСХАЮвЙњжаЖЋВПЕиЧјЁЃЦфжа,ЦћГЕЮВЦјКЭШМУКЮВЦјЪЧдьГЩЮэіВЬьЦјЕФдвђжЎвЛЁЃ
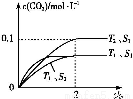
ЃЈ1ЃЉЦћГЕЮВЦјОЛЛЏЕФжївЊдРэЮЊ2NOЃЈgЃЉ+2COЃЈgЃЉ 2CO2ЃЈgЃЉ+N2ЃЈgЃЉЁЃдкУмБеШнЦїжаЗЂЩњИУЗДгІЪБ,cЃЈCO2ЃЉЫцЮТЖШЃЈTЃЉЁЂДпЛЏМСЕФБэУцЛ§ЃЈSЃЉКЭЪБМфЃЈtЃЉЕФБфЛЏЧњЯп,ШчЭМЫљЪОЁЃ
2CO2ЃЈgЃЉ+N2ЃЈgЃЉЁЃдкУмБеШнЦїжаЗЂЩњИУЗДгІЪБ,cЃЈCO2ЃЉЫцЮТЖШЃЈTЃЉЁЂДпЛЏМСЕФБэУцЛ§ЃЈSЃЉКЭЪБМфЃЈtЃЉЕФБфЛЏЧњЯп,ШчЭМЫљЪОЁЃ
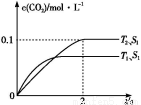
ОнДЫХаЖЯ:
ЂйИУЗДгІЪЧЁЁЁЁЁЁЁЁЗДгІЃЈЬюЁАЗХШШЁБЛђЁАЮќШШЁБЃЉЁЃ
ЂкдкT2ЮТЖШЯТ,0ЁЋ2 sФкЕФЦНОљЗДгІЫйТЪvЃЈN2ЃЉ=ЁЁЁЁЁЁЁЁЁЃ
ЂлЕБЙЬЬхДпЛЏМСЕФжЪСПвЛЖЈЪБ,діДѓЦфБэУцЛ§ПЩЬсИпЛЏбЇЗДгІЫйТЪЁЃШєДпЛЏМСЕФБэУцЛ§S1>S2,дкЩЯЭМжаЛГіcЃЈCO2ЃЉдкT1ЁЂS2ЬѕМўЯТДяЕНЦНКтЙ§ГЬжаЕФБфЛЏЧњЯпЁЃ
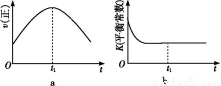
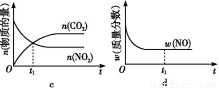
ЂмШєИУЗДгІдкОјШШЁЂКуШнЕФУмБеЬхЯЕжаНјаа,ЯТСаЪОвтЭМе§ШЗЧвФмЫЕУїЗДгІдкНјааЕНt1ЪБПЬДяЕНЦНКтзДЬЌЕФЪЧЁЁЁЁЁЁЃЈЬюДњКХЃЉЁЃ
ЃЈ2ЃЉжБНгХХЗХУКШМЩеВњЩњЕФбЬЦјЛсв§Ц№бЯжиЕФЛЗОГЮЪЬтЁЃ
ЂйУКШМЩеВњЩњЕФбЬЦјКЌЕЊЕФбѕЛЏЮя,гУCH4ДпЛЏЛЙдNOxПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЁЃ
Р§Шч:CH4ЃЈgЃЉ+2NO2ЃЈgЃЉ N2ЃЈgЃЉ+CO2ЃЈgЃЉ+2H2OЃЈgЃЉІЄH=-867 kJ/mol
N2ЃЈgЃЉ+CO2ЃЈgЃЉ+2H2OЃЈgЃЉІЄH=-867 kJ/mol
2NO2ЃЈgЃЉ N2O4ЃЈgЃЉЁЁІЄH=-56.9 kJ/mol
N2O4ЃЈgЃЉЁЁІЄH=-56.9 kJ/mol
аДГіCH4ЃЈgЃЉДпЛЏЛЙдN2O4ЃЈgЃЉЩњГЩN2ЃЈgЃЉКЭH2OЃЈgЃЉЕФШШЛЏбЇЗНГЬЪН:ЁЁ ЁЃ
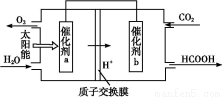
ЂкНЋШМУКВњЩњЕФЖўбѕЛЏЬМЛиЪеРћгУ,ПЩДяЕНЕЭЬМХХЗХЕФФПЕФЁЃШчЭМЪЧЭЈЙ§ШЫЙЄЙтКЯзїгУ,вдCO2КЭH2OЮЊдСЯжЦБИHCOOHКЭO2ЕФдРэЪОвтЭМЁЃДпЛЏМСbБэУцЗЂЩњЕФЕчМЋЗДгІЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЂлГЃЮТЯТ,0.1 mol/LЕФHCOONaШмвКpHЮЊ10,дђHCOO-ЦНКтГЃЪ§Kh=ЁЁЁЁЁЁЁЁЁЃ
ЃЈ1ЃЉЂйЗХШШЃЈ2ЗжЃЉЁЁЂк0.025 mol/ЃЈLЁЄsЃЉЃЈ2ЗжЃЉ
Ђл
 ЃЈ2ЗжЃЉ
ЃЈ2ЗжЃЉ
ЂмbdЃЈ2ЗжЃЉ
ЃЈ2ЃЉЂйCH4ЃЈgЃЉ+N2O4ЃЈgЃЉ N2ЃЈgЃЉ+CO2ЃЈgЃЉ+2H2OЃЈgЃЉЁЁІЄH=-810.1 kJ/mol
N2ЃЈgЃЉ+CO2ЃЈgЃЉ+2H2OЃЈgЃЉЁЁІЄH=-810.1 kJ/mol
ЃЈ2ЗжЃЉ
ЂкCO2+2H++2e- HCOOHЃЈ2ЗжЃЉ
HCOOHЃЈ2ЗжЃЉ
Ђл1.0ЁС10-7ЃЈ2ЗжЃЉ
ЁОНтЮіЁПЃЈ1ЃЉЂйИљОнЭМЯёжЊ,ЁАЯШЙеЯШЦНЪ§жЕДѓЁБЕУT1>T2,Щ§ИпЮТЖШ,CO2ЕФХЈЖШНЕЕЭ,ЦНКтЯђФцЗДгІЗНЯђвЦЖЏ,ЫЕУїе§ЗДгІЪЧЗХШШЗДгІЁЃЂкЯШИљОнЭМЯёМЦЫуCO2ЕФЗДгІЫйТЪ,vЃЈCO2ЃЉ= =0.05 mol/ЃЈLЁЄsЃЉ,ЭЌвЛЛЏбЇЗДгІжаЭЌвЛЪБМфЖЮФк,ИїЮяжЪЕФЗДгІЫйТЪжЎБШЕШгкМЦСПЪ§жЎБШ,ЙЪvЃЈN2ЃЉ=0.025 mol/ЃЈLЁЄsЃЉЁЃЂлДпЛЏМСНгДЅУцЛ§дНДѓЗДгІЫйТЪдНДѓ,ЙЪT1ЁЂS2ЕФЧњЯпдкT1ЁЂS1ЕФЯТЗН,ДпЛЏМСЖдЛЏбЇЦНКтЮогАЯь,ЙЪT1ЁЂS2ЪБcЃЈCO2ЃЉгыT1ЁЂS1ЪБЯрЕШЁЃЂмЗДгІДяЕНЦНКтзДЬЌЪБ,ИїЮяжЪЕФЗДгІЫйТЪВЛдйБфЛЏ,aДэЮѓ;ИУЗДгІдкОјШШЁЂКуШнЕФУмБеЬхЯЕжаНјаа,ЯрЕБгкЩ§ИпЮТЖШ,ЕБЮТЖШВЛБфЪБ,ЛЏбЇЦНКтГЃЪ§ВЛБф,bе§ШЗ;гЩЭМЯёПЩжЊ,CO2КЭNOЮяжЪЕФСПЯрЕШЪБ,ИУЗДгІЮДДяЕНЦНКтзДЬЌ,cДэЮѓ;ЗДгІДяЕНЦНКтзДЬЌЪБ,ИїЮяжЪЕФжЪСПЗжЪ§ВЛдйЗЂЩњБфЛЏ,dе§ШЗЁЃ
=0.05 mol/ЃЈLЁЄsЃЉ,ЭЌвЛЛЏбЇЗДгІжаЭЌвЛЪБМфЖЮФк,ИїЮяжЪЕФЗДгІЫйТЪжЎБШЕШгкМЦСПЪ§жЎБШ,ЙЪvЃЈN2ЃЉ=0.025 mol/ЃЈLЁЄsЃЉЁЃЂлДпЛЏМСНгДЅУцЛ§дНДѓЗДгІЫйТЪдНДѓ,ЙЪT1ЁЂS2ЕФЧњЯпдкT1ЁЂS1ЕФЯТЗН,ДпЛЏМСЖдЛЏбЇЦНКтЮогАЯь,ЙЪT1ЁЂS2ЪБcЃЈCO2ЃЉгыT1ЁЂS1ЪБЯрЕШЁЃЂмЗДгІДяЕНЦНКтзДЬЌЪБ,ИїЮяжЪЕФЗДгІЫйТЪВЛдйБфЛЏ,aДэЮѓ;ИУЗДгІдкОјШШЁЂКуШнЕФУмБеЬхЯЕжаНјаа,ЯрЕБгкЩ§ИпЮТЖШ,ЕБЮТЖШВЛБфЪБ,ЛЏбЇЦНКтГЃЪ§ВЛБф,bе§ШЗ;гЩЭМЯёПЩжЊ,CO2КЭNOЮяжЪЕФСПЯрЕШЪБ,ИУЗДгІЮДДяЕНЦНКтзДЬЌ,cДэЮѓ;ЗДгІДяЕНЦНКтзДЬЌЪБ,ИїЮяжЪЕФжЪСПЗжЪ§ВЛдйЗЂЩњБфЛЏ,dе§ШЗЁЃ
ЃЈ2ЃЉЂйНЋЕквЛИіЗНГЬЪНМѕШЅЕкЖўИіЗНГЬЪНЕУ:CH4ЃЈgЃЉ+N2O4ЃЈgЃЉ N2ЃЈgЃЉ+CO2ЃЈgЃЉ+2H2OЃЈgЃЉ
N2ЃЈgЃЉ+CO2ЃЈgЃЉ+2H2OЃЈgЃЉ
ІЄH=-810.1 kJ/molЁЃ
ЂкДпЛЏМСbБэУцЩЯCO2ЕУЕчзгКЭH+ЗДгІЩњГЩHCOOH,ЫљвдЗЂЩњЕФЕчМЋЗДгІЪНЮЊ:CO2+2H++2e- HCOOHЁЃ
HCOOHЁЃ
ЂлГЃЮТЯТ,0.1 mol/LЕФHCOONaШмвКЕФpHЮЊ10,ШмвКжаOH-ХЈЖШЮЊ
10-4 mol/L,
гЩHCOO-+H2O HCOOH+OH-
HCOOH+OH-
Ц№ЪМЃЈmol/LЃЉ0.100
ЦНКтЃЈmol/LЃЉ0.1-10-4Ёж0.110-410-4
ЕУ:Kh=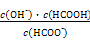 =
=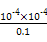 =1.0ЁС10-7ЁЃ
=1.0ЁС10-7ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇЫеНЬАцзмИДЯА зЈЬт12ЮяжЪНсЙЙгыаджЪСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЯТУцгаЙиОЇЬхЕФа№ЪіжаЃЌВЛе§ШЗЕФЪЧ(ЁЁЁЁ)
AЃЎН№ИеЪЏЮЊЭјзДНсЙЙЃЌгЩЙВМлМќаЮГЩЕФЬМдзгЛЗжаЃЌзюаЁЕФЛЗЩЯга6ИіЬМдзг
BЃЎТШЛЏФЦОЇЬхжаЃЌУПИіNaЃЋжмЮЇОрРыЯрЕШЕФNaЃЋЙВга6Иі
CЃЎТШЛЏяЄОЇЬхжаЃЌУПИіCsЃЋжмЮЇНєСк8ИіClЃ
DЃЎИЩБљОЇЬхжаЃЌУПИіCO2ЗжзгжмЮЇНєСк12ИіCO2Зжзг
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇЫеНЬАцзмИДЯА зЈЬт10ЛЏбЇЪЕбщЛљДЁСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЙигкЯТСаИїЪЕбщзАжУЕФа№ЪіжаЃЌе§ШЗЕФЪЧ(ЁЁЁЁ)
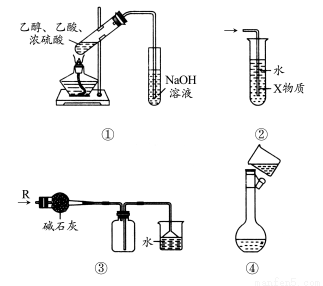
AЃЎзАжУЂйжЦБИввЫсввѕЅ
BЃЎзАжУЂкжаXШєЮЊCCl4ЃЌПЩгУгкЮќЪеNH3ЛђHClЃЌВЂЗРжЙЕЙЮќ
CЃЎзАжУЂлПЩгУгкИЩдяЁЂЪеМЏCl2ЃЌВЂЮќЪеЖргрЕФCl2
DЃЎзАжУЂмХфжЦвЛЖЈЮяжЪЕФСПХЈЖШЕФШмвКЪБзЊвЦвКЬх
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇУћЪІИпПМФЃФтбнСЗСЗЯАОэЃЈBЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКЬюПеЬт
жаЙњеўИЎГаХЕ,ЕН2020Фъ,ЕЅЮЛGDPЖўбѕЛЏЬМХХЗХБШ2005ФъЯТНЕ40%ЁЋ50%ЁЃ
ЃЈ1ЃЉгааЇМѕЬМЕФЪжЖЮжЎвЛЪЧНкФм,ЯТСажЦЧтЗНЗЈзюНкФмЕФЪЧЁЁЁЁЁЁЁЁЁЃ
A.ЕчНтЫЎжЦЧт:2H2O 2H2Ёќ+O2Ёќ
2H2Ёќ+O2Ёќ
B.ИпЮТЪЙЫЎЗжНтжЦЧт:2H2O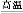 2H2Ёќ+O2Ёќ
2H2Ёќ+O2Ёќ
C.ЬЋбєЙтДпЛЏЗжНтЫЎжЦЧт:2H2O 2H2Ёќ+O2Ёќ
2H2Ёќ+O2Ёќ
D.ЬьШЛЦјжЦЧт:CH4+H2O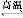 CO+3H2
CO+3H2
ЃЈ2ЃЉCO2ПЩзЊЛЏГЩгаЛњЮяЪЕЯжЬМбЛЗЁЃдкЬхЛ§ЮЊ1 L ЕФУмБеШнЦїжа,ГфШы1 mol CO2КЭ3 mol H2,вЛЖЈЬѕМўЯТЗДгІ:CO2ЃЈgЃЉ+3H2ЃЈgЃЉ CH3OHЃЈgЃЉ+H2OЃЈgЃЉЁЁІЄH=-49.0 kJ/mol,ВтЕУCO2КЭCH3OHЃЈgЃЉЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЁЃ
CH3OHЃЈgЃЉ+H2OЃЈgЃЉЁЁІЄH=-49.0 kJ/mol,ВтЕУCO2КЭCH3OHЃЈgЃЉЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЁЃ
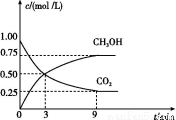
ЂйДг3 minЕН9 min,vЃЈH2ЃЉ=ЁЁЁЁЁЁЁЁmol/ЃЈLЁЄminЃЉЁЃ
ЂкФмЫЕУїЩЯЪіЗДгІДяЕНЦНКтзДЬЌЕФЪЧЁЁЁЁЁЁЁЁЃЈЬюБрКХЃЉЁЃ
A.ЗДгІжаCO2гыCH3OHЕФЮяжЪЕФСПХЈЖШжЎБШЮЊ1ЁУ1ЃЈМДЭМжаНЛВцЕуЃЉ
B.ЛьКЯЦјЬхЕФУмЖШВЛЫцЪБМфЕФБфЛЏЖјБфЛЏ
C.ЕЅЮЛЪБМфФкЯћКФ3 mol H2,ЭЌЪБЩњГЩ1 mol H2O
D.CO2ЕФЬхЛ§ЗжЪ§дкЛьКЯЦјЬхжаБЃГжВЛБф
ЃЈ3ЃЉЙЄвЕЩЯ,CH3OHвВПЩгЩCOКЭH2КЯГЩЁЃВЮПМКЯГЩЗДгІCOЃЈgЃЉ+2H2ЃЈgЃЉ CH3OHЃЈgЃЉЕФЦНКтГЃЪ§:
CH3OHЃЈgЃЉЕФЦНКтГЃЪ§:
ЮТЖШ/Ёц | 0 | 100 | 200 | 300 | 400 |
ЦНКтГЃЪ§ | 667 | 13 | 1.9ЁС1 | 2.4ЁС1 | 1ЁС1 |
ЯТСаЫЕЗЈе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЃ
A.ИУЗДгІе§ЗДгІЪЧЗХШШЗДгІ
B.ИУЗДгІдкЩ§ИпЮТЖШЪБ,CH3OHЃЈgЃЉЕФЬхЛ§ЗжЪ§МѕаЁ,ЫЕУїvе§ЃЈCH3OHЃЉМѕаЁ,vФцЃЈCH3OHЃЉдіДѓ
C.дкT ЁцЪБ,1 LУмБеШнЦїжа,ЭЖШы0.1 mol COКЭ0.2 mol H2,ДяЕНЦНКтЪБ,COзЊЛЏТЪЮЊ50%,дђДЫЪБЕФЦНКтГЃЪ§ЮЊ100
D.ЙЄвЕЩЯВЩгУЩдИпЕФбЙЧПЃЈ5 MpaЃЉКЭ250 Ёц,ЪЧвђЮЊДЫЬѕМўЯТ,дСЯЦјзЊЛЏТЪзюИп
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇУћЪІИпПМФЃФтбнСЗСЗЯАОэЃЈBЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЯТСаЙигкгаЛњЮяЕФЫЕЗЈжа,ВЛе§ШЗЕФЪЧЃЈЁЁ ЁЁЃЉ
A.МзЭщЁЂБНЁЂввДМЖМФмЗЂЩњШЁДњЗДгІ
B.ввЯЉЪЙфхЫЎКЭЫсадИпУЬЫсМиШмвКЭЪЩЋЕФЗДгІРраЭЯрЭЌ
C.гЭжЌдкМюадЬѕМўЯТЕФЫЎНтЗДгІЪЧЙЄвЕжЦЗЪдэЕФдРэ
D.вјАБШмвКЛђаТжЦCuЃЈOHЃЉ2аќзЧвКОљФмМьбщЬЧФђВЁШЫФђвКжаЕФЦЯЬбЬЧ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇУћЪІИпПМФЃФтбнСЗСЗЯАОэЃЈAЃЉЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ФГЭЌбЇгУЯТСазАжУжЦБИВЂМьбщCl2ЕФаджЪЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈЁЁ ЁЁЃЉ
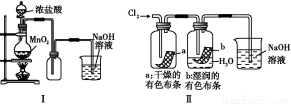
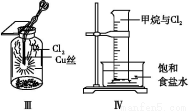
A.ЂёЭМжа:ШчЙћMnO2Й§СП,бЮЫсПЩШЋВПБЛЯћКФ
B.ЂђЭМжа:ЪЊШѓЕФгаЩЋВМЬѕЭЪЩЋ,жЄУїCl2гаЦЏАзад
C.ЂѓЭМжа:ЩњГЩзиЩЋЕФЙЬЬх,жЄУїCl2гаЧПбѕЛЏад
D.ЂєЭМжа:ЙтееКѓСПЭВжаЦјЬхЬхЛ§МѕаЁ,ЫЕУїМзЭщгыCl2ЗЂЩњСЫМгГЩЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇУћЪІбЁдёЬтзЈСЗ РызгЗДгІСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЛЏбЇгУгяЪЧбЇЯАЛЏбЇЕФЙЄОпКЭЛљДЁЁЃЯТСагаЙиЛЏбЇгУгяЕФЪЙгУе§ШЗЕФЪЧ(ЁЁЁЁ)
A.гУЪГДзГ§ШЅЫЎКјФкЕФЫЎЙИ:CaCO3+2H+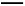 Ca2++CO2Ёќ+H2O
Ca2++CO2Ёќ+H2O
B.ДПМюШмвКГЪМюадЕФдвђЪЧ:C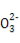 +2H2O
+2H2O H2CO3+2OH-
H2CO3+2OH-
C.ИжЬњЗЂЩњЮќбѕИЏЪДЕФе§МЋЗДгІЪН: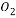 +4e-+2H2O
+4e-+2H2O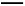 4OH-
4OH-
D.БэЪОЧтЦјШМЩеШШЕФШШЛЏбЇЗНГЬЪНЮЊ2H2(g)+O2(g)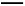 2H2O(l)ЁЁІЄH=-571.6 kJЁЄ mol-1
2H2O(l)ЁЁІЄH=-571.6 kJЁЄ mol-1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇУћЪІбЁдёЬтзЈСЗ ЕчНтжЪШмвКСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
НЋЬњТСЗЏ[Al2Fe(SO4)4ЁЄxH2O]ШмгкЫЎжа,ЕУЕНЧГТЬЩЋШмвК,гаЙиИУШмвКЕФа№Ъіе§ШЗЕФЪЧ(ЁЁ ЁЁ)
A.ЬњТСЗЏгаОЛЫЎзїгУ,ЦфЫЎШмвКЯджаад
B.ИУШмвКжа:2c(Al3+)+c(Fe2+)+c(H+)=4c(S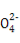 )+c(OH-)
)+c(OH-)
C.дкПеЦјжа,ИУШмвКеєИЩВЂзЦЩе,зюКѓЫљЕУЕФВаСєЙЬЬхЮЊAl2O3ЁЂFe2O3
D.ЯђИУШмвКжаМгШыBa(OH)2ШмвК,ЕБS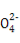 ЭъШЋГСЕэЪБ,Al3+ЁЂFe2+ЧЁКУБЛЭъШЋГСЕэ
ЭъШЋГСЕэЪБ,Al3+ЁЂFe2+ЧЁКУБЛЭъШЋГСЕэ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК2014ИпПМЛЏбЇУћЪІбЁдёЬтзЈСЗ ЛЏбЇгыSTSEСЗЯАОэЃЈНтЮіАцЃЉ ЬтаЭЃКбЁдёЬт
ЦјКђБфЛЏКЭЛЗОГЮЪЬтШЋЧђЙизЂЁЃвдЯТзіЗЈгаРћгкБЃЛЄЛЗОГЕФЪЧ(ЁЁЁЁ)
A.вАЭтЗйЩеРЌЛј
B.ЪЙгУвЛДЮадФОжЪПъзг
C.ДѓСПЪЙгУЛЏЗЪЁЂХЉвЉ
D.ЭЦЙуЪЙгУЩЂзАЫЎФр
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com