
【题目】物质A—J间的转化关系如下图所示,A、C为金属氧化物,其中A为红棕色粉末,B、D是生活中常见金属单质,F、J是难溶于水的白色化合物,G、J受热后容易分解

(1)A的化学式是_________,A与B反应的反应类型是________(填四大基本反应类型)。
(2)I→J反应的离子方程式是___________________________________________。
(3)F转化为G的过程中观察到的现象是__________,反应的化学方程式是____________。
【答案】 Fe2O3 置换反应 AlO2-+CO2+3H2O=Al(OH)3↓+HCO3- 白色沉淀迅速变为灰绿色,逐渐变为红褐色 4Fe(OH)2 + 2H2O + O2 == 4 Fe(OH)3
【解析】A为红棕色粉末,B、D是生活中常见金属单质,该反应是B在高温下发生铝热反应,所以A为Fe2O3,B为Al,生成的C既能与酸反应又能与碱反应,则C为Al2O3,D为Fe,C与盐酸反应生成H为AlCl3,C与氢氧化钠反应生成I为NaAlO2,I与二氧化碳反应生成J为Al(OH)3,J受热分解生成C,D与盐酸反应生成E为FeCl2,E与氢氧化钠反应生成F为Fe(OH)2,F在空气中被氧化生成G为Fe(OH)3,G受热解得A,符合各物质转化关系。
(1)根据上面的分析可知,则A为Fe2O3,A与B的反应为铝热反应,属于置换反应,故答案为:Fe2O3;置换反应;
(2)I为NaAlO2,J为Al(OH)3,偏铝酸钠溶液中通入过量的二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,反应的离子方程式为AlO2-+CO2+3H2O=Al(OH)3↓+HCO3-,故答案为:AlO2-+CO2+3H2O=Al(OH)3↓+HCO3-;
(3)F为Fe(OH)2,F在空气中被氧化生成G为Fe(OH)3,F转化为G的过程中观察到的现象是 白色沉淀迅速变为灰绿色,逐渐变为红褐色,反应的化学方程式是4Fe(OH)2+2H2O+O2═4Fe(OH)3,故答案为:白色沉淀迅速变为灰绿色,逐渐变为红褐色;4Fe(OH)2+2H2O+O2═4Fe(OH)3。


科目:高中化学 来源: 题型:
【题目】微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图所示.下列有关微生物电池的说法错误的是( ) 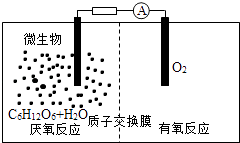
A.正极反应中有CO2生成
B.微生物促进了反应中电子的转移
C.质子通过交换膜从负极区移向正极区
D.电池总反应为C6H12O6+6O2═6CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组制取氯酸钾。制取实验结束后,取出生成了氯酸钾的试管冷却结晶、过滤、洗涤。请简述洗涤氯酸钾晶体的操作__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,某稀溶液中由水电离产生的c(OH-)=10-12mol/L。下列有关该溶液的叙述正确的是
A. 该溶液一定呈酸性
B. 该溶液中的c(H+)可能等于10-3
C. 该溶液的pH可能为2,可能为12
D. 该溶液有可能呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应是旧键断裂和新键形成的过程。共价键的键能是两种原子间形成1 mol共价键(或其逆过程)时释放(或吸收)的能量。已知下面化学键的键能: H—H Br—Br H—Br 键能(kJ·mol-1) 436 193 366,则Br2(g)+H2(g)=2HBr(g)的反应热ΔH等于( )
A. -183 kJ·mol-1B. 183 kJ·mol-1C. -103 kJ·mol-1D. 103 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:

请回答下列问题:
(1)固体a的化学式为________。
(2)写出Ⅱ中加过量的烧碱涉及到的反应离子方程式______________、_____________;Ⅲ中通入足量CO2气体发生反应的离子方程式为_________________。
(3)由Ⅲ中得到滤液c的实验操作为__________,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)________、冷却结晶、过滤洗涤。
(4)滤液c显________性,日常生活中常用其溶质来________________(任写一点);
(5)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3和H2SO4的物质的量之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液加入铝可以生成H2,则在该溶液中一定能大量存在的离子组是( )
A. K+、Cu2+、NO![]() 、Cl- B. K+、Na+、Br-、Cl-
、Cl- B. K+、Na+、Br-、Cl-
C. K+、Ca2+、HCO![]() 、Cl- D. Na+、Mg2+、Br-、SO
、Cl- D. Na+、Mg2+、Br-、SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液和100mL 0.5mol/L CaCl2溶液所含的Cl-物质的量浓度相同的是
A. 500mL 0.1mol/L MgCl2溶液 B. 100mL 0.5mol/L AlCl3溶液
C. 50mL 1mol/L NaCl溶液 D. 25mL 0.5mol/L HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应:4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=﹣1025kJmo1﹣l . 若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
A.
B.
C.
D.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com