
【题目】25℃时,用0.0500molL﹣1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000molL﹣1NaOH溶液所得滴定曲线如图.下列说法正确的是( ) 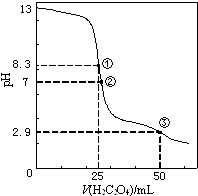
A.点①所示溶液中:c(H+)+c(H2C2O4)+c(HC2O4﹣)=c(OH﹣)
B.点②所示溶液中:c(HC2O4﹣)+2c(C2O42﹣)=c(Na+)
C.点③所示溶液中:c(Na+)>c(HC2O4﹣)>c(H2C2O4)>c(C2O42﹣)
D.滴定过程中可能出现:c(Na+)>c(C2O42﹣)=c(HC2O4﹣)>c(H+)>c(OH﹣)
【答案】BD
【解析】解:A.点①所示的溶液的体积25mL,草酸和氢氧化钠恰好完全反应,生成正盐草酸钠,草酸钠水解,所以溶液中,c(Na+)═2c(HC2O4﹣)+2c(H2C2O4)+2c(C2O42﹣)①,根据电荷守恒得:关系式为:c(Na+)+c(H+)═c(HC2O4﹣)+c(OH﹣)+2c(C2O42﹣)②,将①代入②得:c(H+)+2c(H2C2O4)+c(HC2O4﹣)=c(OH﹣),故A错误;
B.点②溶液中,溶液呈中性,c(H+)=c(OH﹣)①,根据电荷守恒得:关系式为:c(Na+)+c(H+)═c(HC2O4﹣)+c(OH﹣)+2c(C2O42﹣)②,将①代入②得c(HC2O4﹣)+2c(C2O42﹣)=c(Na+),故B正确;
C.点③所示的溶液的体积50mL,草酸过量,溶液溶质为NaHC2O4 , 溶液呈酸性,草酸氢根离子的电离大于草酸氢根离子的水解,所以c(Na+)>c(HC2O4﹣)>c(C2O42﹣)>c(H2C2O4),故C错误;
D.点①为草酸钠成碱性,点②溶液呈中性为草酸钠、草酸氢钠,点③溶液呈酸性,介于②和③之间,随着草酸的滴入,NaHC2O4逐渐增多,所以可出现c(Na+)>c(C2O42﹣)=c(HC2O4﹣)>c(H+)>c(OH﹣),故D正确;
故选BD.
25℃时,用0.0500molL﹣1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000molL﹣1NaOH溶液,发生的反应为:H2C2O4+2NaOH=Na2C2O4+2H2O、H2C2O4+Na2C2O4=2NaHC2O4 .
A.点①表示滴入25.00mL0.0500molL﹣1H2C2O4(二元弱酸)溶液,恰好完全反应,生成正盐草酸钠,结合电荷守恒判断;
B.点②溶液中,溶液呈中性,c(H+)=c(OH﹣),结合电荷守恒判断;
C.点③滴入0.0500molL﹣1H2C2O4(二元弱酸)溶液50.00mL,溶液溶质为NaHC2O4 , 溶液呈酸性;
D.点①为草酸钠成碱性,点②溶液溶质为NaHC2O4、Na2C2O4呈中性,点③溶液,溶质为NaHC2O4 , 呈酸性,介于②和③之间溶液NaHC2O4逐渐增多,溶液呈酸性.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.用FeCl3溶液腐蚀铜板:Fe3++Cu═Fe2++Cu2+
B.向氨水中通入过量SO2:SO2+2NH3?H2O═2NH4++SO32﹣+H2O
C.用MnO2与浓盐酸反应制Cl2:MnO2+4HCl ![]() ?Mn2++2Cl﹣+Cl2↑+2H2O
?Mn2++2Cl﹣+Cl2↑+2H2O
D.在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO﹣+2Fe(OH)3+4OH﹣═2FeO43﹣+3Cl﹣+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G对多种植物病原菌具有抑制作用,由丙酮合成G的路线如下: 
(1)写出化合物G中含氧官能团的名称 .
(2)反应②的类型为 .
(3)反应①还会得到另一产物H,其分子式为C8H14O2 , 写出H的结构简式 .
(4)反应⑦生成的G会部分转化为另一产物I,Ⅰ为链状结构,分子式为C10H18O4 , 写出Ⅰ的结构简式:
(5)一分子G消去一分子水可得物质J,写出同时满足下列条件的J的一种同分异构体的结构简式: ①能与FeCl3溶液发生显色反应;②分子的核磁共振氢谱有2个峰.
(6)以CH3OH、CH≡CH为原料合成聚丙烯醇 ![]() ,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2
,写出合成流程图(无机试剂任用).合成流程图示例如下:CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOHCH3COO﹣+H+ , 要使溶液中 ![]() 值增大,可以采取的措施是( )
值增大,可以采取的措施是( )
A.加少量烧碱溶液
B.降低温度
C.加少量冰醋酸
D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图象的解释或得出结论正确的是( ) 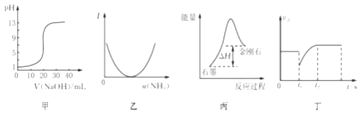
A.图甲表示0.10molL﹣1NaOH溶液滴定20.00 mL 0.10 molL﹣1醋酸溶液的滴定曲线
B.图乙表示向乙酸溶液中通入氨气至过量过程中溶液导电性I的变化
C.根据图丙所示可知:石墨转化为金刚石吸收热量,石墨比金刚石稳定
D.图丁表示反应2SO2+O22SO3 , t1时刻只减小了 SO3的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F是一种治疗关节炎止痛药,合成F的一种传统法路线如图: 
(1)B中含氧官能团的名称为 .
(2)C→D的反应可分为两步,其反应类型为、 .
(3)写出比F少5个碳原子的同系物X的结构简式:(写一种);X有多种同分异构体,满足下列条件的X的同分异构体共有种. ①属于芳香族化合物 ②苯环上只有1个取代基 ③属于酯类物质
(4)写出E转化为F和无机盐的化学方程式: .
(5)已知: ① ![]() ②
② ![]() (R、R′表示烃基)
(R、R′表示烃基)
合成F的一种改良法是以2﹣甲基﹣1﹣丙醇[(CH3)2CHCH2OH)]、苯、乙酸酐[(CH3CO)2O]为原料来合成,写出有关的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
H2C=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如:Cu(OH)2 ![]() Cu2++2OH﹣ , Ksp=c(Cu2+)[c(OH﹣)]2=2×10﹣20 . 当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
Cu2++2OH﹣ , Ksp=c(Cu2+)[c(OH﹣)]2=2×10﹣20 . 当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.
(1)某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于 .
(2)要使0.2molL﹣1CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们所形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为__________;Y元素原子最外层电子的电子排布图为__________。
(2)若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为__________(填“共价键”或“离子键”)。
(3)该化合物的立体构型为__________,中心原子的杂化类型为__________,分子为__________(填“极性分子”或“非极性分子”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com