
| A. | 铁和稀盐酸反应 2Fe+6H+═2Fe3++3H2↑ | |
| B. | 碳酸钙溶于稀盐酸中 CO32-+2H+═CO2+H2O | |
| C. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 碳酸氢钠溶液与盐酸反应 HCO3-+H+═CO2↑+H2O |
分析 A.铁与稀盐酸反应生成的是亚铁离子;
B.碳酸钙为难溶物,离子方程式中不能拆开;
C.次氯酸不能拆开,应该保留分子式;
D.碳酸氢钠与盐酸反应生成氯化钠、二氧化碳气体和水.
解答 解:A.铁和稀盐酸反应生成氯化亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故A错误;
B.碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故B错误;
C.氯气与水反应生成氯化氢和次氯酸,次氯酸不能拆开,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故C错误;
D.碳酸氢钠溶液与盐酸反应的离子方程式为:HCO3-+H+═CO2↑+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸、浓盐酸、氨水、乙醚、丙酮等易挥发的药品必须严密封存 | |
| B. | 化学药品室或准备室内可存放大量的碳化钙、黄磷、汽油、二甲苯、镁等物品 | |
| C. | 氯化钙、氯化铁、氯化亚铁、硝酸铵等易潮解的药品必须存放于干燥的室内,瓶口盖紧后用蜡或火漆封闭,在存放的橱中放入干燥剂 | |
| D. | 对于危险品必须遵守公安部门关于危险品的采购、保管和使用的有关规定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
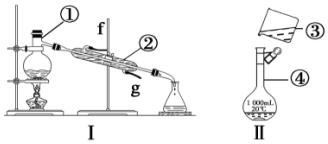
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃容器可长期盛放各种酸 | |
| B. | 水中加入明矾、硫酸铁溶液可以起净水作用 | |
| C. | Al2O3可制造耐高温的实验仪器 | |
| D. | Na2S可除去污水中有毒的Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素符号 | K | L | M | Q | R | T | N |
| 原子半径/nm | 0.186 | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 | 0.152 |
| 主要化合价 | +1 | +2 | +3 | +6,-2 | +2 | -2 | +1 |
| A. | K、L、M三种元素的单质的还原性逐渐增强 | |
| B. | 在RCl2分子中,各原子最外层均满足8电子的稳定结构 | |
| C. | Q元素的最高价氧化物为电解质,其水溶液能够导电 | |
| D. | K在T单质中燃烧所得的化合物中有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
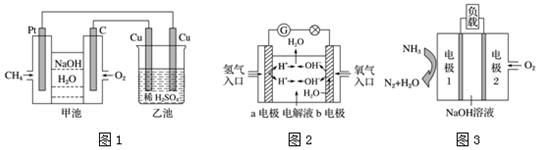
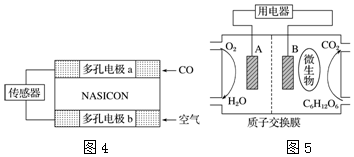
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
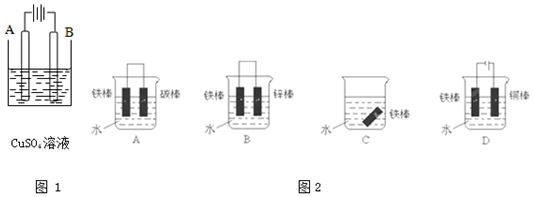
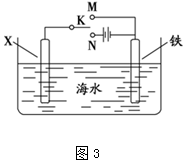
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com