
���� CH3COOHΪ������ʣ�����Һ�в��ֵ��룬HCl��ǿ����ʣ�����Һ����ȫ���룬
��1��pH=-lgc��H+����Ũ����ͬ����ҺpH��С����Һ��������Ũ�ȴ�С���������жϣ�
��2��pH��ͬ��Һ��������Ũ����ͬ�����ݴ��������ᣬ������ǿ������жϣ�
��3���к͵����������ƣ����ݻ�ѧ����ʽ�еĵ����ϵ�����жϣ�
��4����Һ���������ʵ�����ͬʱ����Ӧ����Һ�����ԣ���������������жϣ�
��5����������Ϊǿ�ᣬ��Һ����ȫ���룬����Ϊ������ʣ���Һ�в��ֵ��������
��6������ϡ������������������Ũ�Ȼ������䣬������ϡ�ͺ����̶���������жϣ�
��� �⣺��1��������pH��ͬʱ����Һ��������Ũ����ͬ�������ṩ1mol/L�������ӣ���Ҫ����Ũ��Ӧ����1mol/L����Ҫ�Ȼ�����ҺŨ��Ϊ1mol/L�����������ʵ���Ũ���ɴ�С���е��ǣ��٣��ڣ���ѡA��
��2�������ǵ����ʵ���Ũ����ͬʱ��CH3COOH�����Ჿ�ֵ��룬������Ũ����С��HCl��ǿ����ȫ���룬����������Ӵ��ڴ��ᣬ����pH=-lgc��H+����֪����Һ��pH�ɴ�С���е��ǣ��٣��ڣ���ѡA��
��3���к���ͬ�������ͬ���ʵ���Ũ�ȵ��ռ���Һ�����������������ʵ���Ϊ1mol����Ҫ����1mol����ҪHCl 1mol������ͬ���ʵ���Ũ�ȵ���������Һ�������С��ϵΪ����=�ڣ���ѡC��
��4�������Ũ����ͬ�Ģ١�����Һ����������Ϊ1mol���ֱ���ͬŨ�ȵ��ռ���Һ��Ӧ��Ҫʹ��Ӧ����Һ��pHΪ7��CH3COOH�����ᣬǡ���к����ɴ�������Һ�ʼ��ԣ�������Ҫ�ռ�С��1mol���Ȼ����1mol��������ǡ�÷�Ӧ��Һ�����ԣ����������ռ���Һ������ɴ�С��ϵΪ���ڣ��٣���ѡB��
��5�������ǵ�pH��ͬ�����ͬʱ������Ϊ������ʣ������Ũ�ȴ������ᣬ����ͬʱ��������п������������������٣��ڣ���ѡA��
��6����pH��ͬ���������ϡ��10���������������ӵ����ʵ����������䣬��������ϡ�����У�����̶�������Һ�����������ʵ���������Һ��pHС��������Һ�ģ�����pH��ϵΪΪ���ڣ��٣���ѡB��
���� ���⿼������Ӧ����Һ���ʼ���ҺpH���㣬��Ŀ�Ѷ��еȣ������Դ�ע�����Ϊ���������Һ�в��ֵ��롢����ΪһԪǿ�ᣬ���������ǿ�����ض�ѧ��������û���֪ʶ���ʵ�������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.01 mol•L-1��H2A��Һ | |
| B�� | 0.01 mol•L-1NaHA��Һ | |
| C�� | 0.02 mol•L-1HCl��Һ��0.04 mol•L-1NaHA��Һ�������� | |
| D�� | 0.02mol•L-1 NaOH��Һ0.02 mol•L-1 NaHA��Һ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ���ķ���ʽ��C8H8 | B�� | �뱽��ϩ 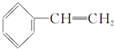 ��Ϊͬ���칹�� ��Ϊͬ���칹�� | ||
| C�� | �����ܷ����ӳɷ�Ӧ | D�� | ���Ķ���ȡ���ﹲ��4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
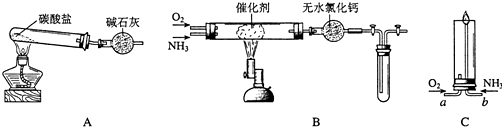
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������NaHCO3��Na2CO3�ķֱ�������������ȫ��Ӧ��Na2CO3������CO2�� | |
| B�� | 84g NaHCO3��106g Na2CO3�ֱ���ͬŨ������������ȫ��Ӧ��Na2CO3�����������NaHCO3���� | |
| C�� | ������ʯ��ˮ��CaCl2��Һ�ֱ�����������Һ�У���ֻ��Na2CO3�������� | |
| D�� | ͨ������£�Na2CO3���ܽ�ȴ���NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com