
Ąė×Ó¼ü”¢¹²¼Ū¼ü”¢ŗĶ·¶µĀ»ŖĮ¦ŹĒ¹¹³ÉĪļĪ¢Į£Ö®¼äµÄ²»Ķ¬×÷ÓĆĮ¦”£ĻĀĮŠĪļÖŹÖŠÖ»ŗ¬ÓŠÉĻŹöŅ»ÖÖ×÷ÓĆĮ¦µÄŹĒ
A”¢±ł B”¢ĀČ»ÆÄĘ C”¢ĒāŃõ»ÆÄĘ D”¢µā
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
A.C60ŹĒŅ»ÖÖŠĀµÄ»ÆŗĻĪļ£¬¾ßÓŠČ«²æÓɹ²¼Ū¼ü×é³ÉµÄæÕ¼äĶųד½į¹¹
B.C60ŗĶŹÆÄ«¶¼ŹĒĢ¼µÄĶ¬ĖŲŅģŠĪĢå
C.C60ÖŠŗ¬Ąė×Ó¼ü”¢¹²¼Ū¼ü”¢ÅäĪ»¼ü
D.C60µÄĻą¶Ō·Ö×ÓÖŹĮæŹĒ720£¬“ęŌŚ·¶µĀ»ŖĮ¦£¬ČŪ·Šµć½ĻµĶ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
[»Æѧ-ĪļÖŹ½į¹¹ÓėŠŌÖŹ]13·Ö
£Ø1£©ŌŖĖŲµÄµŚŅ»µēĄėÄÜ£ŗAl Si£ØĢī”°>”±»ņ£ŗ”°<”±£©
£Ø2£©»łĢ¬Mn2+µÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ ”£
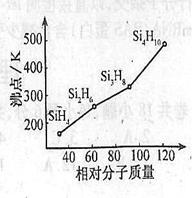
£Ø3£©¹čĶé£ØSinH2n+2£©µÄ·ŠµćÓėĘäĻą¶Ō·Ö×ÓÖŹĮæµÄ±ä»Æ¹ŲĻµČēÓŅĶ¼ĖłŹ¾£¬³ŹĻÖÕāÖÖ±ä»Æ¹ŲĻµµÄŌŅņŹĒ ”£
£Ø4£©ÅšÉ°ŹĒŗ¬½į¾§Ė®µÄĖÄÅšĖįÄĘ£¬ĘäŅõĄė×ÓXm”Ŗ£Øŗ¬B”¢O”¢HČżÖÖŌŖĖŲ£©µÄĒņ¹÷Ä£ŠĶČēÓŅĻĀĶ¼ĖłŹ¾£ŗ
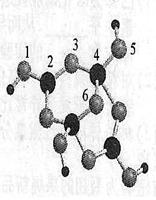
¢ŁŌŚXm”ŖÖŠ£¬ÅšŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶÓŠ £»ÅäĪ»¼ü“ęŌŚÓŚ Ō×ÓÖ®¼ä£ØĢīŌ×ӵďż×Ö±źŗÅ£©£»
m= £ØĢīŹż×Ö£©”£
¢ŚÅšÉ°¾§ĢåÓÉNa+”¢Xm”ŖŗĶH2O¹¹³É£¬ĖüĆĒÖ®¼ä“ęŌŚµÄ×÷ÓĆĮ¦ÓŠ £ØĢīŠņŗÅ£©”£
A£®Ąė×Ó¼ü B.¹²¼Ū¼ü C.½šŹō¼ü
D.·¶µĀ»ŖĮ¦ E.Ēā¼ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģø£½ØŹ”ø߶žÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
µŖŌŖĖŲæÉŅŌŠĪ³É¶ąÖÖ·Ö×ÓŗĶĄė×Ó£¬ČēNH3”¢N2H4”¢N3£”¢NH4+”¢N2H62+µČ”£»Ų“šŅŌĻĀĪŹĢā£ŗ
£Ø1£©NµÄ»łĢ¬Ō×ÓÖŠ£¬ÓŠ øöŌĖ¶ÆדĢ¬²»Ķ¬µÄĪ“³É¶Ōµē×Ó”£
£Ø2£©Ä³ŌŖĖŲŌ×ÓÓėN3£ŗ¬ÓŠĻąĶ¬µÄµē×ÓŹż£¬Ę仳Ģ¬Ō×ӵļŪµē×ÓÅŲ¼Ź½ŹĒ_______”£
£Ø3£©NH3”¢N2H4”¢NH4+”¢N2H62+ĖÄÖÖĪ¢Į£ÖŠ£¬Ķ¬ÖÖĪ¢Į£¼äÄÜŠĪ³ÉĒā¼üµÄÓŠ____________£»²»ÄÜ×÷ĪŖÅäĪ»ĢåµÄÓŠ____________”£
£Ø4£©“浞µŖĖįHN3ŌŚ³£ĪĀĻĀŹĒŅ»ÖÖŅŗĢ壬·Šµć½Ļøߣ¬ĪŖ308.8K£¬Ö÷ŅŖŌŅņ ŹĒ ”£
£Ø5£©ėĀ(N2H4)·Ö×ÓæÉŹÓĪŖNH3·Ö×ÓÖŠµÄŅ»øöĒāŌ×Ó±»”ŖNH2(°±»ł)Č”“śŠĪ³ÉµÄĮķŅ»ÖÖµŖµÄĒā»ÆĪļ”£
¢ŁN2H4·Ö×ÓÖŠµŖŌ×ÓµÄŌÓ»ÆĄąŠĶŹĒ______”£
¢ŚėĀæÉÓĆ×÷»š¼żČ¼ĮĻ£¬Č¼ÉÕŹ±·¢ÉśµÄ·“Ó¦ŹĒ£ŗN2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)
ČōøĆ·“Ó¦ÖŠÓŠ4 mol N”ŖH¼ü¶ĻĮŃ£¬ŌņŠĪ³ÉµÄ¦Š¼üÓŠ________mol”£
£Ø6£©ėĀÄÜÓėĮņĖį·“Ӧɜ³ÉN2H6SO4”£N2H6SO4»ÆŗĻĪļĄąŠĶÓėĮņĖįļ§ĻąĶ¬£¬ŌņN2H6SO4 ÄŚĪ¢Į£¼ä×÷ÓĆĮ¦²»“ęŌŚ_______(Ģī±źŗÅ£©
a.Ąė×Ó¼ü b.¹²¼Ū¼ü c.ÅäĪ»¼ü d.·¶µĀ»ŖĮ¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012½ģ¼ŖĮÖŹ”ø߶žĻĀŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĖµ·Ø£¬ÕżČ·µÄŹĒ
A.Ąė×Ó¼ü¾ßÓŠ±„ŗĶŠŌŗĶ·½ĻņŠŌ
B.·¶µĀ»ŖĮ¦ŹĒ·Ö×Ó¼ä×÷ÓĆĮ¦µÄŅ»ÖÖ£¬Ēā¼ü²»ŹōÓŚ·Ö×Ó¼ä×÷ÓĆĮ¦
C.s¹ģµĄÓės¹ģµĄÖ®¼äæÉŅŌŌŚČĪŗĪ·½ĻņÉĻ³É¼ü£¬ĖłŅŌ¹²¼Ū¼ü¶¼Ć»ÓŠ·½ĻņŠŌ
D.s¹ģµĄÓėp¹ģµĄÖ»ÓŠŃŲ×ÅŅ»¶ØµÄ·½Ļņ£¬²ÅÄÜ·¢Éś×ī“ó³Ģ¶ČµÄÖŲµž£¬ŠĪ³É¹²¼Ū¼ü
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com