
向浓度相等、体积均为50 mL的A、B两份NaOH溶液中 ,分别通入一定量的CO2后,再稀释到100 mL。
,分别通入一定量的CO2后,再稀释到100 mL。
(1)在NaOH溶液中通入一定量的CO2后,溶液中溶质的可能组成是
①________,②________,③________,④________。
(2)在稀释后的溶液中逐滴加入0.1 mol/L的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示。

①A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是________mL(标准状况)。
②B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为________。
③原NaOH溶液的物质的量浓度为________。
科目:高中化学 来源:2016-2017学年河北省高一12月月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3·H2O+H2O
B.实验室配制的亚铁盐溶液在空气中被氧化:4Fe2++O2+2H2O=4Fe3++4OH-
C.向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH- NH3↑+H2O
NH3↑+H2O
D.用酸化的高锰酸钾溶液氧化双氧水:2 MnO4-+6H++H2O2===2Mn2++3O2↑+4H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北定州中学高一承智班12月月考化学卷(解析版) 题型:选择题
下列离子方程式不正确的是
A.NaHSO4溶液中加入过量Ba(OH)2溶液:H++SO42-+Ba2++OH-=BaSO4↓+H2O
B.次氯酸钙溶液中加入亚硫酸钠:SO32-+Ca2+=CaSO3↓
C.NH4HCO3溶液中加足量NaOH溶液共热:HCO3-+NH4++2OH-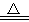 CO32-+NH3↑+2H2O
CO32-+NH3↑+2H2O
D.硫酸亚铁溶液中加入用硫酸酸化的双氧水:2Fe2++2H++H2O2=2Fe3++2H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:选择题
下列各组离子能在呈酸性的无色溶滚中大量共存的是( )
A.Ba2+、Na+、NO3-、SO42- B.Mg2+、Cl-、Al3+、SO42-
C .K+\、OH-、HCO3-、NO3- D.NH4+、Na+、Fe2+、MnO4-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上期中化学卷(解析版) 题型:选择题
下列实验操作或设计中,可行的是( )
A. CO2通入足量BaCl2溶液中,产生白色沉淀
B. 除去O2中混有的H2,可将气体通过灼热CuO
C. 利用分液斗可分离酒精和氯化钠的混合物
D. 加稀盐酸后过滤,除去铜扮中没有的少量镁粉和铝粉
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一12月月考化学卷(解析版) 题型:选择题
一定量的Na2O2与CO2反应后的固体物质41.8 g,恰好与1 L 1 mol·L-1的稀盐酸完全反应,下列说法正确的是( )
A.41.8 g固体物质为Na2CO3
B.41.8 g固体物质为0.1 mol Na2CO3和0.4 mol Na2O2的混合物
C.41.8 g固体物质为31.2 g NaHCO3和10.6 g Na2CO3的混合物
D.一定量的Na2O2为78 g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一12月月考化学卷(解析版) 题型:选择题
下列各组中的两种物质作用时,反应条件(温度、反应物用量比)改变,不会引起产物的种类改变的是( )
A.Na和O2 B.NaOH和CO2
C.Na2O2和CO2 D.NaHCO3和Ca(OH)2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二12月月考化学卷(解析版) 题型:选择题
对于常温下pH=1的硝酸溶液,有关叙述:
①该溶液1mL稀释至100mL后,pH=3
②向该溶液中加入等体积、pH=13的氢氧化钡溶液恰好完全中和
③该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为1×10﹣12
④向该溶液中加入等体积、等浓度的氨水,所得溶液pH=7
其中正确的是( )
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:填空题
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)的分解反应。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)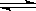 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表 :
:
温度/℃ | 15 | 20 | 25 | 30 | 35 |
平衡总压强/kPa | 5.7 | 8.3 | 12 | 17.1 | 24 |
平衡气体 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
①该可逆反应的平衡常数的表达式为________________________
②可以判断该分解反应已经达到平衡的是________。
A.2v(NH3)=v(CO2)
B.密闭容器中混合气体的密度不变
C.密闭容器中CO2的体积分数不变
D.密闭容器中总压强不变
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25 ℃下达到分解平衡。若在恒温下增大容器体积,氨基甲酸铵固体的质量将________(填“增加”、“减少”或“不变”)。
④该反应的焓变ΔH_________0(填“>”、“=”或“<”)
(2)在高温下一氧化碳可将二氧化硫还原为单质硫。
已知:①C(s)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1
②CO2(g)+C(s)===2CO(g) ΔH2=+172.5 kJ·mol-1
③S(s)+O2(g)===SO2(g) ΔH3=-296.0 kJ·mol-1
请写出CO与SO2反应的热化学方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com