
【题目】功能高分子P的合成路线如图:

(1)A的分子式是C7H8,其结构简式是_____。
(2)试剂a是____。
(3)反应③的化学方程式:___。
(4)化合物H属于A的同系物,其分子式为C8H10,其同分异构体共有___种,其中___(写结构简式)的一氯代物只有两种。
【答案】 浓HNO3和浓H2SO4
浓HNO3和浓H2SO4  +NaOH
+NaOH![]()
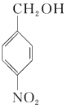 +NaCl 4
+NaCl 4 ![]()
【解析】
采用逆推法,由高分子P的结构简式,以及A的分子式,可以推出D为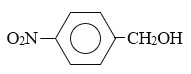 ,G为
,G为 ,由D可推知C为
,由D可推知C为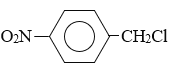 ,由C可推知B为
,由C可推知B为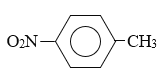 ,则A为甲苯,据此分析推断;
,则A为甲苯,据此分析推断;
采用逆推法,由高分子P的结构简式,以及A的分子式,可以推出D为 ,G为
,G为 ,由D可推知C为
,由D可推知C为 ,由C可推知B为
,由C可推知B为 ,则A为甲苯,据此分析推断;
,则A为甲苯,据此分析推断;
(1)根据上述分析,A为甲苯,其结构简式为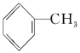
答案为 ;
;
(2)B→C发生取代,氯原子取代甲基上的氢,反应③为水解反应,因此反应①为取代反应,在甲基的对位上引入-NO2,即试剂a为浓硝酸、浓硫酸;
答案为浓硝酸、浓硫酸;3
(3)根据上述分析,反应③发生水解反应,即反应方程式为: +NaOH
+NaOH![]()
 +NaCl;
+NaCl;
答案为 +NaOH
+NaOH![]()
 +NaCl;
+NaCl;
(4)A为甲苯,则C8H10为苯的同系物,其同分异构体为C6H5CH2CH3,将乙基看成两个甲基,在苯环上的位置是邻、间、对,共有4 种;一氯代物有两种,说明有两种不同的氢原子,该结构属于对称结构,即符合条件的结构简式为![]() ;
;
答案为4种;![]() 。
。


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
【题目】向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)已知碘元素最终变为无色HIO3。上述整个过程中的还原剂是_______________________。写出CCl4层变成紫色的离子反应方程式________________________________________。
(2)若把KI换成KBr,则CCl4层变为_________色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是______________________________________。
(3)智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘。试配平该反应的化学方程式,并用短线标出电子转移方向及总数__NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+_H2O,已知含氧酸盐的氧化作用随溶液酸性的加强而增强,在制备试验时,定时取样,并用酸化的氯化钡来检测SO42-离子生成的量,发现开始阶段反应速度呈递增的趋势,试简述这变化趋势发生的原因:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D 4种可溶性盐,它们的阳离子可能分别是Ca2+、Ag+、Na+、Cu2+中的某一种,阴离子可能分别是NO3-、SO42-、Cl-、CO32-中的某一种。
①若把4种盐分别溶解于盛有蒸馏水的4支试管中,均得澄清溶液,只有B盐的溶液呈蓝色。
②若向①的4支试管中分别加盐酸,C溶液中有沉淀产生,A溶液中有无色无味气体逸出。
(1)根据①②的事实推断B、C的化学式分别为_________、___________
(2)写出A与D反应的化学方程式:______________________________________;
(3)若想从A与D反应后的混合物中分别提取两种固体产物,需要进行的实验操作是_________和________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于臭氧性质的叙述中,不正确的是
A.臭氧比氧气的氧化性更强,常温下能将银、汞等较不活泼的金属氧化
B.臭氧是比氯水更好的消毒剂,因为它在消灭细菌后变成O2,无污染
C.臭氧和活性炭一样,能够吸附有机色素,是种很好的漂白剂
D.臭氧和氧气在一定条件下可以相互转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,2.24LHF含分子数目为0.1NA
B. 120 g NaHSO4固体含有H+的数目为NA
C. 100mL0.1mol/L的Na2CO3溶液中,含阴离子的数目大于0.01NA
D. 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子交换法净化水过程如图所示。下列说法中错误的是

A. 经过阳离子交换树脂后,水中阳离子的总数不变
B. 水中的![]() 、
、![]() 、Cl通过阴离子树脂后被除去
、Cl通过阴离子树脂后被除去
C. 通过净化处理后,水的导电性降低
D. 阴离子树脂填充段存在反应H++OH![]() H2O
H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物结构和性质的说法错误的是
A. 分子式为C5H10O2且能与 NaHCO3反应放出气体的结构共有4种
B. 石油是混合物,可通过分馏得到汽油、煤油等纯净物
C. 苯甲酸(![]() )分子中所有原子可能位于同一平面
)分子中所有原子可能位于同一平面
D. 1mol盐酸美西律( )最多可与3 mol H2发生加成
)最多可与3 mol H2发生加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有密度为1.25 g·mL-1,质量分数为36.5%的浓盐酸,现需240mL0.1mol·L-1的盐酸,请回答下列问题:
(1)浓盐酸的物质的量浓度为_____。
(2)配制0.1 mol·L-1的盐酸应用量筒量取浓盐酸体积____mL。
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次,并将所缺内容填在横线上)______。
A.用30 mL蒸馏水洗涤____ 2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用 _____加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线____处
(4)若实验过程中出现如下情况,所配溶液浓度将会怎样?(填偏高或偏低)
①加蒸馏水时不慎超过刻度线_____②量取浓盐酸时仰视______③定容时俯视_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯


(1)制备粗品
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是___________,导管B除了导气外还具有的作用是___________。
②试管C置于冰水浴中的目的是____________________________________________。
(2)制备精品

①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按如图装置蒸馏,蒸馏时要加入生石灰,目的是__________________。
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是(______)
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
(4)设计实验检验环己烯精品中是否含己二醛_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com