
| A. | NH5的电子式: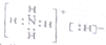 | |
| B. | NH5中N元素的化合价为+5价 | |
| C. | 1molNH5中含有5molN-H键 | |
| D. | 1molNH5与H2O完全反应,转移电子2mol |
分析 NH5属于离子化合物,是由铵根离子与氢负离子通过离子键结合而成,反应NH5+H2O=NH3•H2O+H2↑中NH5的H元素化合价由-1价变为0价、水中H元素化合价由+1价变为0价,所以NH5作还原剂,水作氧化剂,据此解答.
解答 解:A.NH5属于离子化合物,是由铵根离子与氢负离子通过离子键结合而成,电子式为: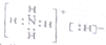 ,故A正确;
,故A正确;
B.NH5中N元素的化合价为-3价,故B错误;
C..NH5是离子化合物氢化铵,所以1molNH5中有4NA个N-H键,故C错误;
D.1 mol NH5与H2O完全反应,转移电子的物质的量=1mol×[0-(-1)]=1mol,故D错误;
故选:A.
点评 本题考查了物质的结构及性质,熟悉离子化合物与共价化合物的区别及氧化还原反应规律是解题关键,注意氨根离子中存在配位键,题目难度不大.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源:2017届湖南省长沙市高三上学期第三次月考模拟化学试卷 题型:选择题
下列各表述与示意图一致的是

A.图①表示25℃时,用0.1mol/L盐酸滴定20mL0.1mol/LNaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线
B.图②表示一定条件下进行的反应2SO2(g)+O2(g) 2SO3(g)△H<O各成分的物质的量变化.t2时刻改变的条件可能是降低温度或缩小容器体积
2SO3(g)△H<O各成分的物质的量变化.t2时刻改变的条件可能是降低温度或缩小容器体积
C.图③表示某明矶溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(0H)2溶液体积的关系,在加入20mL溶液时铝离子恰好沉淀完全
D.图④表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=+183kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤 | B. | 石油 | C. | 天然气 | D. | 生物质能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2悬浊液 | 金属钠 | |
| A | 中和反应 | - | 溶解 | 产生氢气 |
| B | - | 有银镜 | 加热后有砖红色沉淀 | 产生氢气 |
| C | 水解反应 | 有银镜 | 加热后有砖红色沉淀 | - |
| D | 水解反应 | - | - | - |
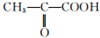 ),由以上事实推知乳酸的结构简式为CH3CH(OH)COOH.
),由以上事实推知乳酸的结构简式为CH3CH(OH)COOH.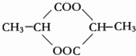 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2、H2、NH3在容器中共存 | B. | N2、H2、NH3的浓度不改变 | ||
| C. | 反应已达到化学平衡状态 | D. | N2、H2完全转化为NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ③⑤ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 核外电子排布相同的微粒化学性质也相同 | |
| C. | 同主族元素从上到下,单质的熔点逐渐降低 | |
| D. | 同族上下相邻两种元素的原子序数之差可能为32 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 马口铁(镀锡铁)镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 2CaCO3(s)+2SO2(g)+O2(g)═2CaSO4(s)+2CO2(g)在高温下能自发进行,则该反应的△H>0 | |
| C. | 恒温恒容密闭容器中进行的反应N2(g)+3H2(g)?2NH3(g);△H=a kJ•mol-1,平衡时向容器中再充入N2和H2,反应速率加快,a值不变 | |
| D. | 氢硫酸(弱酸)中加入少量CuSO4溶液(H2S+CuSO4═CuS↓+H2SO4),H2S的电离程度和溶液的pH均增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com