
| A. | 等质量的乙醛和乙酸乙酯完全燃烧时消耗氧气的量不相等 | |
| B. | 淀粉水解的最终产物在加热条件下可与新制氢氧化铜反应生成砖红色沉淀 | |
| C. | 可用饱和碳酸钠溶液除去乙酸乙酯中的乙酸 | |
| D. | 2-氯-2-甲基丙烷在氢氧化钠的醇溶液中加热可生成甲基丙烯 |
分析 A、乙醛和乙酸乙酯的最简式均为CH2O;
B、淀粉水解的最终产物为葡萄糖,含-CHO;
C、饱和碳酸钠可与乙酸反应,并降低乙酸乙酯的溶解度;
D、2-氯-2-甲基丙烷在氢氧化钠的醇溶液中加热会发生消去反应,据此回答.
解答 解:A、乙醛和乙酸乙酯的最简式均为CH2O,等质量的乙醛和乙酸乙酯完全燃烧时消耗氧气的量相等,故A正确;
B、淀粉水解的最终产物为葡萄糖,含-CHO,具有还原性,加热条件下与新制氢氧化铜反应生成砖红色沉淀,故B正确;
C、饱和碳酸钠可与乙酸反应,并降低乙酸乙酯的溶解度,则可用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,故C正确;
D、2-氯-2-甲基丙烷在氢氧化钠的醇溶液中加热会发生消去反应,可生成2-甲基-1-丙烯,故D错误.
故选D.
点评 本题考查较综合,涉及有机物的性质、混合物的分离提纯、有机反应等,侧重淀粉、乙酸的性质及乙醛和乙酸乙酯组成的考查,题目难度不大


科目:高中化学 来源: 题型:选择题
| A. | 两个原子或多个原子之间的相互作用叫化学键 | |
| B. | 阴、阳离子间通过静电引力而形成的化学键叫做离子键 | |
| C. | 只有金属元素和非金属元素化合时才能形成离子键 | |
| D. | 离子化合物中一定含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应 | 乙醇(mol) | 乙酸(mol) | 乙酸乙酯(mol) |
| 1 | 2 | 2 | 1.33 |
| 2 | 3 | 2 | 1.57 |
| 3 | 4 | 2 | x |
| 4 | 5 | 2 | 1.76 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 该反应中,热能转化为产物内部的能量 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 断裂旧化学键吸收的总能量小于形成新化学键放出的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③两步都是氧化还原反应 | B. | 只有第②步是氧化还原反应 | ||
| C. | 该方法对生产设备基本没有腐蚀 | D. | 该方法对环境污染较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:O2-<F-<Na+<Li+ | B. | 第一电离能:He<Ne<Ar | ||
| C. | 分子中的键角:CH4>H2O>CO2 | D. | 共价键的键能:C-C<C=C<C≡C |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
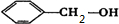 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
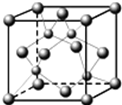 A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D原子的S电子与P电子数相等,E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式回答下列问题:
A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D原子的S电子与P电子数相等,E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式回答下列问题:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com