
【题目】某化学研究性学习小组用CO还原Fe2O3 , 并在实验结束后用磁铁吸出生成的黑色粉末X进行探究. [探究目的]分析黑色粉末X的组成,并进行相关实验.
[查阅资料]
I.CO还原Fe2O3的实验中若温度不同、受热不均时会生成Fe3O4 , 也能被磁铁吸引.
II.Fe3O4+8H+=2Fe3++Fe2++4H2O
(1)[猜想假设]黑色粉末X的组成可能是、 , 或二者的混合物. [实验探究]
编号 | 实验操作 | 实验现象 |
① | 取少量黑色粉末X放入试管中,注入足量的一定浓度的盐酸,微热 | 黑色粉末逐渐溶解,同时有气泡产生,溶液呈浅绿色. |
② | 向上述试管中滴加几滴KSCN溶液,振荡 | 溶液没有呈现红色 |
实验①中产生气泡的离子方程式为 .
(2)根据②中溶液未呈红色,不能推断出黑色粉末X中无Fe3O4 , 请用离子方程式解释原因: .
(3)为了证明黑色粉末X中是否含有Fe3O4 , 该小组进行如图所示实验: 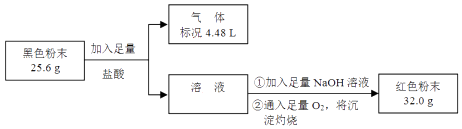
请根据数据分析说明黑色粉末X中是否含有Fe3O4 . .
【答案】
(1)Fe;Fe3O4;Fe+2H+═Fe2++H2↑
(2)Fe3O4+8H+═2Fe3++Fe2++4H2O、Fe+2Fe3+═3Fe2+
(3)方法1:因为32gFe2O3中含Fe元素为22.4g,而25.6g>22.4g,所以X中还含有O元素,还含有Fe3O4; 方法2:因为产生产生4.48L氢气,需要Fe单质为11.2g,而25.6g>11.2g,所以X中还含有Fe3O4
【解析】解:[猜想假设] (1)CO还原Fe2O3为Fe生成的黑色粉末X,Fe、Fe3O4黑色且能被磁铁吸引,则磁性黑色粉末X可能是Fe、Fe3O4、或二者的混合物;所以答案是:Fe、Fe3O4;黑色粉末X与盐酸反应有气泡产生,溶液呈浅绿色,说明铁与盐酸反应生成氢气和氯化亚铁,离子反应为:Fe+2H+═Fe2++H2↑;所以答案是:Fe+2H+═Fe2++H2↑;(2)黑色粉末X与盐酸反应,若铁足量,少量的Fe3O4 , 加盐酸溶解发生反应:Fe3O4+8H+═2Fe3++Fe2++4H2O,因为铁足量,将生成的三价铁还原为亚铁离子:Fe+2Fe3+═3Fe2+ , 不能使KSCN溶液显色,故根据②中溶液未呈红色,不能推断出黑色粉末X中无Fe3O4;所以答案是:Fe3O4+8H+═2Fe3++Fe2++4H2O、Fe+2Fe3+═3Fe2+;(3)方法1:生成的红色粉末为Fe2O332.0g,因为32 g Fe2O3中含Fe元素为 ![]() g=22.4 g,而25.6 g>22.4 g,所以X中还含有O元素,还含有Fe3O4;方法2:因为产生4.48L氢气,氢气为0.2mol,Fe单质为0.2mol×56g/mol=11.2 g,而25.6 g>11.2 g,所以X中还含有Fe3O4;所以答案是:方法1:因为32 g Fe2O3中含Fe元素为22.4 g,而25.6 g>22.4 g,所以X中还含有O元素,还含有Fe3O4;方法2:因为产生产生4.48L氢气,需要Fe单质为11.2 g,而25.6 g>11.2 g,所以X中还含有Fe3O4 .
g=22.4 g,而25.6 g>22.4 g,所以X中还含有O元素,还含有Fe3O4;方法2:因为产生4.48L氢气,氢气为0.2mol,Fe单质为0.2mol×56g/mol=11.2 g,而25.6 g>11.2 g,所以X中还含有Fe3O4;所以答案是:方法1:因为32 g Fe2O3中含Fe元素为22.4 g,而25.6 g>22.4 g,所以X中还含有O元素,还含有Fe3O4;方法2:因为产生产生4.48L氢气,需要Fe单质为11.2 g,而25.6 g>11.2 g,所以X中还含有Fe3O4 .


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】将一定量纯净的氨基甲酸铵固体置于特制的密优真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡NH2COONH4(s) ![]() 2NH3(g)+CO2(g),若保持温度和容器体积不变,再充入n (NH3): n (CO)=2:1,则再次达到平衡时c (NH3)
2NH3(g)+CO2(g),若保持温度和容器体积不变,再充入n (NH3): n (CO)=2:1,则再次达到平衡时c (NH3)
A. 增大 B. 不变 C. 变小 D. 因条件不足无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式是
A.向氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
B.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
C.碳酸氢钠溶液与硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O
D.硫酸铝溶液中加入过量氨水: Al3++3OH-=Al(OH)3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可用作分析试剂、鞣革还原剂、脱氯剂等.它受热、遇酸易分解.它有多种制备方法,其中硫化碱法为:向热的硫化钠和亚硫酸钠混合液中通入二氧化硫,经吸硫、蒸发、结晶,制得硫代硫酸钠晶体.制备过程中发生的主要反应如下: Na2S+H2O+SO2→Na2SO3+H2S …(i)
2H2S+SO2→3S+2H2O …(ii)
S+Na2SO3 ![]() Na2S2O3 …(iii)
Na2S2O3 …(iii)
(1)已知Na2S2O3分解反应是吸热反应,由此可得出:该分解反应中,反应物断裂化学键所吸收的总能量(填“大于”、“小于”或“等于”)生成物形成化学键所放出的总能量.
(2)Na2S2O3具有还原性,判断依据是、(至少写出两条).
(3)上述反应i~iii总反应的化学方程式为 . 制备过程中,即使将反应物的用量按化学方程式的计量数进行配比,反应后各反应物仍有剩余,这说明该过程中存在 .
(4)为了保证硫代硫酸钠的产量,生产中通入的SO2不能过量,原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】英国会议员代表团曾到广州、东莞、深圳考察,来中国取经“碳捕捉“技术,希望能与广东省合作开发潮汐能。科学家利用NaOH溶液“捕捉”空气中的CO2,反应过程如图所示。下列有关说法不正确的是
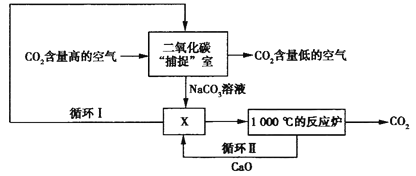
A. 图中循环I 中的物质是NaOH
B. 图中X中物质分离的基本操作是蒸发结晶
C. 二氧化碳“捕捉”室中,将NaOH溶液进行“喷雾”,有利于对CO2的吸收
D. 用该方法捕提到的CO2还可用来制备甲醇等产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数值.下列有关叙述正确的是( )
A.1 mol D2O分子所含的中子数为8NA
B.48 g氧气和臭氧的混合气体中的氧原子数为3NA
C.11.2 L 甲烷(CH4)中的共价键数为2NA
D.1 mol N2与3 mol H2反应生成的NH3分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤矿的矿井里为了防止“瓦斯”(甲烷)爆炸事故,应采取的安全措施是( )
A.通风并严禁烟火
B.进矿井前先用明火检查是否有甲烷
C.戴防毒面具
D.用大量水吸收甲烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com