
【题目】设NA为阿伏你德罗常数的值,下列说法正确的是
A. 12. 4 g白磷(P4)中所含的P-P键数目为0. 6 NA
B. 40 g SiC晶体中含有SiC分子的数目为NA个
C. 1 mol淀粉(C6H10O5)水解后产生的葡萄糖分子数目为NA
D. 标准状况下,2 mol Na2O2与44.8 L SO2完全反应,转移的电子数目为2NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】1-溴丙烷是一种重要的有机合成中间体,沸点为71℃,密度为1.36 g·cm-3。实验室制备少量1-溴丙烷的主要步骤如下:
步骤1:在仪器A中加入搅拌磁子、12 g正丙醇及20 mL水,冰水冷却下缓慢加入28 mL浓H2SO4;冷却至室温,搅拌下加入24 g NaBr。
步骤2:如图所示搭建实验装置,缓慢加热,直到无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL 5% Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得1-溴丙烷。
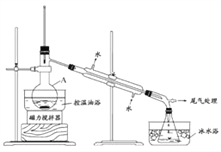
(1)仪器A的名称是_____________;加入搅拌磁子的目的是防止暴沸和___________________。
(2)反应时生成的主要有机副产物有2-溴丙烷和__________________________________。
(3)步骤2中需向接受瓶内加入少量冰水并置于冰水浴中的目的是___________________。
(4)步骤2中需缓慢加热使反应和蒸馏平稳进行,目的是______________________________。
(5)步骤4中用5%Na2CO3溶液洗涤有机相的操作: 向分液漏斗中小心加入12 mL 5% Na2CO3溶液,振荡,____________,静置,分液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<O,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
2SO3(g) △H<O,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是
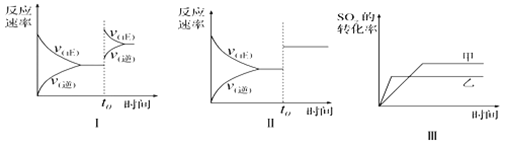
A. 图I研究的是t0时刻增大O2的浓度对反应速率的影响
B. 图II研究的是t0时刻增大压强后对反应速率的影响
C. 图III研究的是催化剂对化学平衡的影响,且甲的催化效率比乙高
D. 图III研究的是温度对化学平衡的影晌.且乙的温度较高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题. 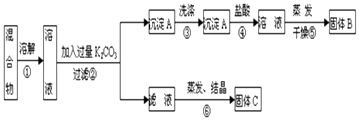
(1)B物质的化学式为 .
(2)在蒸发操作中必须用到蒸发皿,下面对蒸发皿的操作中正确的是
A.将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热
B.将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
C.将蒸发皿放置在三脚架上直接用酒精灯火焰加热
D.在三脚架上放置泥三角,将蒸发皿放置在泥三角上加热
(3)该方案的明显失误是因为某一步设计不当而使分离产物不纯,该步正确的方案可以设计为 .
(4)若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是的质量.
(5)请按要求写出下列离子方程式:
生成沉淀A:
沉淀A与盐酸反应:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A. 在溴水中存在如下平衡:Br2+H2O![]() HBr+HBrO,当加入NaOH溶液后颜色变浅
HBr+HBrO,当加入NaOH溶液后颜色变浅
B. 对2H2O2![]() 2H2O+O2的反应,使用MnO2可加快制O2的反应速率
2H2O+O2的反应,使用MnO2可加快制O2的反应速率
C. 反应CO+NO2![]() CO2+NO ΔH<0,升高温度使平衡向逆反应方向移动
CO2+NO ΔH<0,升高温度使平衡向逆反应方向移动
D. 合成氨反应:N2+3H2![]() 2NH3 ΔH<0,为使氨的产率提高,应采取低温高压的措施
2NH3 ΔH<0,为使氨的产率提高,应采取低温高压的措施
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在.实验室里从海藻中提取碘的流程如图: 海藻 ![]() 海藻灰
海藻灰 ![]() 悬浊液
悬浊液 ![]() 含I﹣的溶液
含I﹣的溶液 ![]() X
X ![]() Y→晶态碘
Y→晶态碘
某化学兴趣小组将上述流程②③设计成如图所示: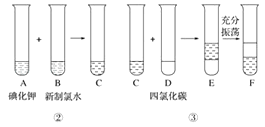
【提示:已知②中发生反应的化学方程式为Cl2+2KI═2KCl+I2】
回答下列问题:
(1)写出提取过程①③中实验操作名称:① , ③ . 根据提示,②中反应(填“是”或“不是”)氧化还原反应.
(2)四氯化碳本身是色、密度比水的液体,它(填“是”或“不是”)电解质.F中下层液体的颜色为色,上层液体中溶质的主要成分为 .
(3)从F中将两层液体进一步分离的操作是 .
(4)在萃取过程中,使用到的(除烧杯和铁架台外)实验仪器有(填序号). A.试管 B.长颈漏斗 C.分液漏斗 D.蒸发皿 E.酒精.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100 mL 6 mol·L-1的H2SO4跟过量锌粉反应,在一定温度下,要想加快反应进行的速率,但又不影响生成的氢气的总量,可向反应物中加入适量的
A. 适量浓H2SO4 B. 铜 C. 醋酸钠固体 D. 硝酸钾溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com