
| A. | 使用催化剂的目的是提高反应物的转化率 | |
| B. | 循环使用N2、H2的目的是提高氨的产率 | |
| C. | 温度控制在500℃左右的目的是有利于化学平衡向正反应方向移动 | |
| D. | 高压下反应有利于增大反应速率,所以压强越高越好 |
分析 A.催化剂对平衡移动无影响;
B.循环使用N2、H2,可使反应物尽可能转化为生成物;
C.合成氨反应为放热反应;
D.压强越大,对设备的要求越高.
解答 解:A.催化剂对平衡移动无影响,则使用催化剂可加快反应速率,对转化率无影响,故A错误;
B.循环使用N2、H2,可使反应物尽可能转化为生成物,则可提高氨的产率,故B正确;
C.合成氨反应为放热反应,温度控制在500℃左右与催化剂活性、反应速率有关,而升高温度合成氨反应逆向移动,故C错误;
D.压强越大,对设备的要求越高,合成氨不能利用较大的压强,故D错误;
故选B.
点评 本题考查化学平衡及应用,为高频考点,把握合成氨反应的特点、平衡移动为解答的关键,侧重分析与应用能力的考查,注意化学反应原理及工业生产的联系,题目难度不大.


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:解答题

 $\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH
$\stackrel{H_{2}O}{→}$2RCOOH ②RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH .
. .
.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴蒸气被活性炭吸附 | B. | 电解水 | ||
| C. | HCl溶解于水 | D. | 打雷放电时,O2变成O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2$\stackrel{Ca(OH)_{2}}{→}$CaSO3$→_{△}^{O_{2}}$CaSO4 | |
| B. | CO2(g)+H2O(g)$→_{叶绿素}^{光}$O2$\stackrel{放电}{→}$O3 | |
| C. | 石油$\stackrel{分馏}{→}$C2H4$\stackrel{催化剂}{→}$ | |
| D. | NaCl水溶液$→_{(惰性电极)}^{通电}$NaOH溶液$\stackrel{Al(OH)_{3}}{→}$NaAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
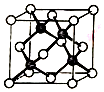 冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或圆心,实心球所示原子位于立方体内)类似.下列有关冰晶胞说法合理的是( )
冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如图,其中空心球所示原子位于立方体的顶点或圆心,实心球所示原子位于立方体内)类似.下列有关冰晶胞说法合理的是( )| A. | 冰晶胞内水分子间以共价键结合 | |
| B. | 晶体冰与金刚石晶体硬度都很大 | |
| C. | 冰分子间的氢键无方向性和饱和性 | |
| D. | 氢键存在导致冰晶胞与金刚石晶胞排列方式类似 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 常压下5种元素的单质中Z单质的熔点最高 | |
| B. | Y、Z的阴离子电子层结构都与R原子的相同 | |
| C. | Y元素的非金属性比W元素的非金属性强 | |
| D. | W的氢化物的还原性比Y的氢化物的还原性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气和二氧化硫均可做漂白剂,若同时使用它们漂白-湿润物质,漂白效果会更好 | |
| B. | 为消除碘缺乏病,卫生部规定食盐必须加碘,其中碘以单质形式存在 | |
| C. | 工业酒精不能勾兑美酒,因其中含有甲醇,饮后会造成人的双目终生失明 | |
| D. | 淀粉、纤维素和油脂都属于天然高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰石与稀盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-=BaSO4↓ | |
| C. | 氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-=Fe(OH)3↓ | |
| D. | 稀硝酸溶液与铜反应:Cu+4H++NO3-=Cu2++2H2O+NO↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃料的燃烧都是放热反应 | |
| B. | 氯化钾的电子式为: | |
| C. | 决定化学反应速率的主要因素是反应物的浓度 | |
| D. | 氯化氢溶于水能电离出H+、Cl-,所以氯化氢是离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com