
| A. | Fe2+的水溶液为浅绿色 | |
| B. | Fe3+的水溶液为黄色 | |
| C. | Fe3+具有氧化性,Fe2+具有还原性 | |
| D. | Fe3+溶液中滴入含KSCN-的溶液,立即出现红色沉淀 |
分析 Fe2+溶于水后呈浅绿色,由于Fe2+处于铁元素的中间价态,故既有氧化性又有还原性;Fe3+溶于水后呈黄色,由于处于铁元素的最高价态,故只有氧化性无还原性,据此分析.
解答 解:A、中学常见水溶液有颜色离子有:Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO4-(紫色),故A正确.
B、Fe3+的水溶液为黄色,故B正确;
C、氧化性是指物质得电子的性质,还原性是指物质失电子的性质,元素处于最高价态时,只表现为氧化性,元素处于最低价态时,只表现为还原性,处于中间价态,既表现氧化性,又表现还原性.如:H2O中H为+1价(最高价态),表现为氧化性,O为-2价(最低价态),表现为还原性,所以H2O既有氧化性,又有还原性;Fe2+处于中间价态,既能得电子,又能失电子,所以既有氧化性,又有还原性.故C正确;
D、Fe3+溶液中滴入SCN-,溶液呈红色,不会出现红色沉淀,故D错误.
故选D.
点评 1、中学常见水溶液有颜色离子有:Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO4-(紫色),
2、氧化性、还原性的判断:最高价态的元素只有氧化性,最低价态元素只有还原性,中间价态的既有氧化性又有还原性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 向水中加人稀氨水,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 向水中加人少量固体NaCl,平衡逆向移动,c(H+)降低 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
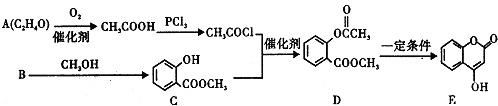
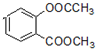 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+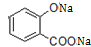 +H2O.
+H2O.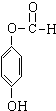 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 原电池的电极材料中必须至少有一极是金属 | |
| C. | 牺牲阳极的阴极保护法是利用了电解原理 | |
| D. | 用电解法精炼铜时,粗铜作阳极,纯铜作阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应中一定有氧元素参与 | |
| B. | 氧化还原反应中所有元素化合价都变化 | |
| C. | 氧化还原反应只有一种元素的化合价变化 | |
| D. | 氧化还原反应中电子有得必有失,化合价有升必有降 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com