
分析 (1)氧化还原反应中,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,根据元素化合价变化计算转移电子数;
(2)有元素化合价降低的物质为氧化剂,还原剂被氧化得到氧化产物,根据方程式计算.
解答 解:(1)该反应中铜元素的化合价变化为0价→+2价,氮元素的化合价变化为+5价→+4价,所以得失电子的最小公倍数是2,所以其电子转移的方向和数目为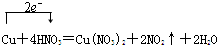 ,
,
故答案为: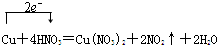 ;
;
(2)在反应Cl2+2KOH═KCl+KClO+H2O中氯气中Cl元素化合价降低,Cl2为氧化剂,化合价升高被氧化得到氧化产物KClO,当有149g即2molKCl产生时,消耗2molCl2,其中被氧化的Cl2为1mol,该反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2;KClO;1;Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查了氧化还原反应,明确元素化合价变化是解本题关键,难点是电子转移的方向和数目的分析,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A>B>C>D>E | B. | B>A>C>D>E | C. | C>D>E>A>B | D. | E>D>C>B>A |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液和CO2的反应 | B. | NaOH溶液和醋酸的反应 | ||
| C. | NaOH溶液和盐酸反应 | D. | 氨水和稀H2SO4的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3比NaHCO3易溶于水 | |
| B. | NaHCO3比Na2CO3稳定 | |
| C. | 石灰水能与NaHCO3反应,但不与Na2CO3反应 | |
| D. | 等质量的Na2CO3和NaHCO3与盐酸反应,消耗HCl的质量比为42:53 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3 和NaOH | B. | Na2CO3和HCl | C. | Na2CO3和H2SO4 | D. | NaCl和AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电负性的大小顺序为Cl>S>P | |
| B. | 由于NO3-和SO3互为等电子体,所以可以推断NO3-的空间构型为平面三角形 | |
| C. | 根据晶格能的大小可以判断MgCl2的熔点比CaCl2高 | |
| D. | 液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com