
A.1 mol 任何物质都约含有6.02×1023个原子
B.0.012 kg12C中含有约6.02×1023个碳原子
C.阿伏加德罗常数的粒子集体就是1 mol
D.使用摩尔表示物质的量时必须指明粒子的名称
A
解析:构成物质的粒子除原子外,还有分子、离子等,所以1 mol物质不是都含有6.02×1023个原子,若是1 mol铝或1 mol氦气,可以这样论。但若是1 mol双原子分子或多原子物质就不同,例如1 mol CaCl2含有1 mol Ca2+(即6.02×1023个Ca2+)和2 mol Cl-(即1.204×1024个Cl-),所以A不正确。0.012 kg12C中所含的碳原子数,即为阿伏加德罗常数,约为6.02×1023,故B选项正确。1 mol任何物质所含粒子数即为阿伏加德罗常数,所以阿伏加德罗常数的集体就是1 mol。摩尔这个单位所表示的对象是粒子,而粒子又包括分子、离子、质子、中子、电子等,所以使用摩尔表示物质的量时必须用化学式指明粒子的名称。例如1 mol O2,不能说1 mol氧气,更不能说1 mol氧。


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
如表是不同pH环境时某浓度铬酸(H2CrO4)溶液中,离子浓度(mol/L)与pH的关系,下列说法错误的是( )
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y |
| Z | W |
| A、Z的原子序数可能是X的两倍 |
| B、单质的活泼性可能是Y<Z |
| C、X、Z的最高价氧化物对应水化物可能均为强酸 |
| D、分别由Y、W形成的单质可能都是原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、反应N2(g)+3H2(g)
| |||||
| B、化学平衡常数、弱电解质的电离平衡常数、溶度积常数均只受温度的影响 | |||||
| C、对于弱电解质的电离平衡常数,当温度一定时,电离平衡常数越小,其酸性越强 | |||||
| D、将AgNO3溶液和KCl溶液混合后,若c(Ag+)?c(Cl-)<KSP(AgCl),则溶液中无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
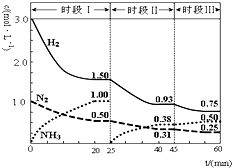 N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示.下列说法错误的是( )
N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ?mol-1.1L密闭恒容容器中,反应体系中各物质浓度随时间变化的曲线如图示.下列说法错误的是( )| A、前20分钟反应物的转化率为50% | B、第25分钟改变的条件是将NH3从反应体系中分离出去 | C、时段Ⅰ仅将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数增大 | D、若第60分钟时反应又达到了平衡,则时段Ⅲ改变的条件是降低温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com