
| A、分子数 | B、密度 |
| C、质量 | D、质子数 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
| B、NH3易液化 |
| C、HF、HCl、HBr、HI的热稳定性依次减弱 |
| D、H2S的熔沸点低于H2O的熔、沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
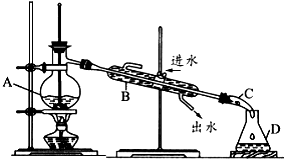
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z的稳定性逐渐增强 |
| B、A、B、C、D只能形成四种单质 |
| C、X、Y、Z三种化合物的熔沸点逐渐升高 |
| D、只含有A、B、C、D 四种元素的化合物有两种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合溶液的pH一定等于7 |
| B、如果混合溶液的pH大于7,则碱一定为弱碱 |
| C、如果碱是强碱,则pH一定大于7 |
| D、如果酸是强酸,则pH一定小于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
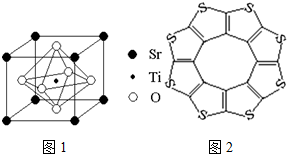 氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.| C-S | C=S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com