
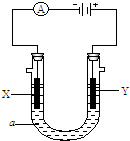
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案科目:高中化学 来源: 题型:
| A、c (Ac-)>c (Cl-)>c (H+)>c (HAc) |
| B、c (Ac-)>c (Cl-)>c (HAc)>c(H+) |
| C、c (Ac-)=c (Cl+)>c (H+)>c (HAc) |
| D、c (Na+)+c (H+)=c (Ac-)+c (Cl-)+c (OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁片放入氯化铁溶液中:Fe+Fe3+═2Fe2+ |
| B、二氧化碳通入碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- |
| C、硫酸铝溶液跟氨水反应:Al3++3NH3?H2O═Al(OH)3↓+3 NH4+ |
| D、氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
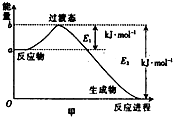 (1)常温下取0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:
(1)常温下取0.2mol/LHCl溶液与0.2mol/LMOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,试回答以下问题:| c(H+)×c(F-) |
| c(HF) |
查看答案和解析>>
科目:高中化学 来源: 题型:
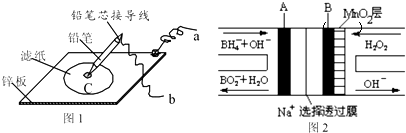
| A、图2电池放电过程中,Na+从正极区向负极区迁移 |
| B、图2电池正极区的电极反应为BH4--8e-+8OH-=BO2-+6H2O |
| C、若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点处出现红色 |
| D、若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是A电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑤ | B、②③④ |
| C、①③⑤ | D、②④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com