
 4NO(g)+6H2O(g)������������ȷ����
4NO(g)+6H2O(g)������������ȷ����| A����Ӧ�ﵽƽ��ʱ�������ַ�Ӧ���ת������ȣ�����ʼͶ���n��NH3����n��O2��=1��1 |
| B����Ӧ�ﵽƽ���������ϵ�г���O2�������NH3��ת���� |
| C����Ӧ�ﵽƽ��ʱ��������ϵ�г���ϡ�����壬�������� |
| D����v����NH3):v����NO��=1��1ʱ��˵���û�ѧ��Ӧ�Ѿ��ﵽƽ�� |
 �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д� �¾�����ĩ���100��ϵ�д�
�¾�����ĩ���100��ϵ�д� ȫ�ܴ���100��ϵ�д�
ȫ�ܴ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(��)����H=Q(Q<0)��һ�������£���Ӧ��Y��ת�����뷴Ӧʱ�䣨t���Ĺ�ϵ����ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ��
2Z(��)����H=Q(Q<0)��һ�������£���Ӧ��Y��ת�����뷴Ӧʱ�䣨t���Ĺ�ϵ����ͼ��ʾ����ʹ����a��Ϊ����b�ɲ�ȡ�Ĵ�ʩ��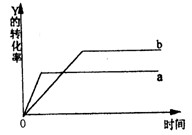
| A���Ӵ��� | B�������¶� | C������ѹǿ | D������Y��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HI(g)��������Ӧ���ȣ������ﵽƽ���t0ʱ�ı䷴Ӧ��ijһ������������������ʵ������䣩�������������ѹǿ��������˵����ȷ���ǣ� ��
2HI(g)��������Ӧ���ȣ������ﵽƽ���t0ʱ�ı䷴Ӧ��ijһ������������������ʵ������䣩�������������ѹǿ��������˵����ȷ���ǣ� ��| A��������������ɫ���ƽ����Է���������С |
| B��ƽ�ⲻ�ƶ�����������ܶ����� |
C���ı�����ǰ���ٶ�ͼ��Ϊ������ͼ�� |
| D��H2ת��������HIƽ��Ũ�ȱ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3C��g����2D��g����(bΪ
3C��g����2D��g����(bΪ 3��������) ��
3��������) �� ��B���� ��
��B���� ��| t�� | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3COO-��H+
CH3COO-��H+ CH3COOH��OH-
CH3COOH��OH- 3COO-)������Һ��pHΪ_______
3COO-)������Һ��pHΪ_______ (����ֵ)��
(����ֵ)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
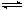 2NH3����ƽ���÷�Ӧ�ų�������Ϊ18.4 kJ����������ܵ����ʵ���Ϊ3.6 mol�������ڵ�ѹǿ��Ϊԭ����90%����֪N2��H2��ת������ͬ��
2NH3����ƽ���÷�Ӧ�ų�������Ϊ18.4 kJ����������ܵ����ʵ���Ϊ3.6 mol�������ڵ�ѹǿ��Ϊԭ����90%����֪N2��H2��ת������ͬ�� ��
�� ��ƽ����ȫ��ͬ��
��ƽ����ȫ��ͬ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3����H��0�ﵽƽ��ı�������������ƽ��(ͼ�к������ʾ��Ӧʱ��, �������ʾ��Ӧ����)
2NH3����H��0�ﵽƽ��ı�������������ƽ��(ͼ�к������ʾ��Ӧʱ��, �������ʾ��Ӧ����) 

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
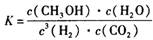 ���¶�����,Kֵ��С������˵����ȷ����
���¶�����,Kֵ��С������˵����ȷ����A���÷�Ӧ�Ļ�ѧ����ʽΪ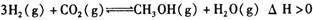 |
| B���ں��¡����ݵ��ܱ�������,�����������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬ |
| C��ƽ��ʱ�������������䣬ʹ�ô�����������CO2��ת�� |
| D���ں��¡����ݵ��ܱ������У�����H2��Ũ��ʱ,CO2��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Z+W���������������������£�����ѹǿ����Ӧ���ʱ仯ͼ����ͼ��ʾ�������X��Y��Z��W�������ʵľۼ�״̬˵����ȷ���ǣ� ��
Z+W���������������������£�����ѹǿ����Ӧ���ʱ仯ͼ����ͼ��ʾ�������X��Y��Z��W�������ʵľۼ�״̬˵����ȷ���ǣ� ��
| A��X��Y��Ϊ���壬Z��W����һ��Ϊ���� |
| B��Z��W����һ�������壬X��Y�Է����� |
| C��X��Y��Z��W�Է����� |
| D��Z��W��Ϊ���壬X��Y����һ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com