
| A、S | B、N2 | C、C | D、Si |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
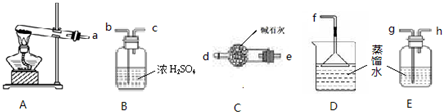
| ||
| ||
| 催化剂 |
| 高温高压 |
| c2(NH3) |
| c(N2)?c3(H2) |
| c2(NH3) |
| c(N2)?c3(H2) |
查看答案和解析>>
科目:高中化学 来源:黄冈重点作业 高一化学(下) 题型:022
某元素X原子的M层比N层多12个电子,它的L层要比M层少6个电子,它有两种常见的阳离子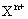 和
和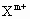 (其中n>m).
(其中n>m).
(1)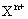 的M层比X的M层少________个电子,
的M层比X的M层少________个电子,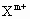 的L层比M层少________个电子,Xn+的稳定性________Xm+的稳定性(填“大于”或“小于”).
的L层比M层少________个电子,Xn+的稳定性________Xm+的稳定性(填“大于”或“小于”).
(2)X单质在氧气中燃烧产物的化学式为________,X单质与硫反应的产物的电子式为________,X单质与稀硫酸反应的离子方程式为________,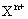 与NaOH溶液反应的离子方程式为________.
与NaOH溶液反应的离子方程式为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是元素周期表的一部分,根据表中的①~⑩中元素,用相关的化学用语填空:
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑩ | ② | ③ | ④ | ⑧ | |||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
(1)元素⑩的名称是______,从元素原子得失电子的角度看,元素④具有____________ (填“氧化性”、“还原性”);比元素⑧质子数多16的元素在周期表中所处位置___ ;
(2)⑥④⑦的氢化物稳定性由弱到强的顺序依次: (写氢化物的化学式);
(3)元素③的气态氢化物与其最高价氧化物的水化物反应的方程式为 ;
(4)写出元素⑤形成的单质在氧气中燃烧产物的电子式_______________,这一反应是___________(填“吸热”、“放热”)反应;元素②和④形成化合物电子式为 ;
(5)用电子式表示①与⑨反应得到的化合物的形成过程___________________________ ;
(6)某元素R的气态氢化物为HXR,且R在该氢化物中的质量分数为94%,8.5g的HXR气体在标准状态下的体积是5.6L。HXR的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com