
| A.①④ | B.①②④ | C.①②④⑤ | D.①②③④ |
 CH3COOH+OH-,有:Kh=
CH3COOH+OH-,有:Kh= =
=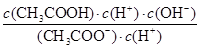 =
=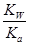 ,故Ka·Kh=Kw;⑤电解精炼铜时,由于粗铜中的较Cu活泼的金属变为金属阳离子进入电解质溶液中,铜离子浓度减小,说法错误。
,故Ka·Kh=Kw;⑤电解精炼铜时,由于粗铜中的较Cu活泼的金属变为金属阳离子进入电解质溶液中,铜离子浓度减小,说法错误。 

科目:高中化学 来源:不详 题型:单选题
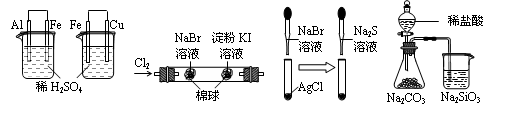
| 实验 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 氧化性:Cl2>Br2>I2 |
| C | 白色固体先变为淡黄色,后变为黑色 | 溶解性:AgCl>AgBr>Ag2S |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
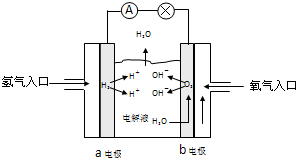
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.因为LiI在水中的溶解度比在有机溶剂中大,所以选用水溶液做电解质 | |||
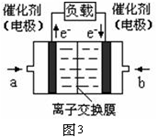
B.电池反应方程式为2Li+I2
| |||
| C.电池的负极为I2 | |||
| D.充电时,阳极反应为2LiI→Li+2I-+2e- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
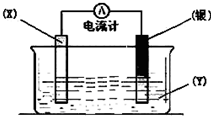
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
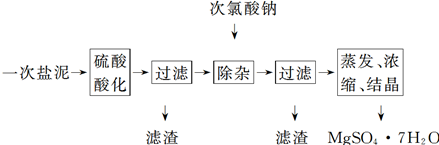
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用反应热数据的大小判断不同反应反应速率的快慢 |
| B.用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.用平衡常数的大小判断化学反应可能进行的程度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CH3OH(g) ΔH
CH3OH(g) ΔH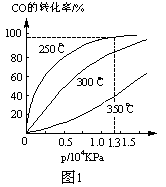
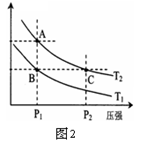
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铅蓄电池在放电过程中,正负极质量均增加 |
| B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H> O |
| C.25℃时,Mg(OH)2固体在20 mL 0.01 mol·L-1氨水中的Ksp比在20 mL 0.01 mol·L-1 NH4Cl溶液中的Ksp小 |
D.将浓度为0.1mol·L-1的HF溶液加水不断稀释,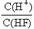 的值始终保持增大 的值始终保持增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com