
【题目】氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义。回答下列问题:
(1)肼(N2H4)与四氧化二氮分别是火箭发射器中最常用的燃料与氧化剂。已知3.2g液态肼与足量液态四氧化二氮完全反应,生成氮气和液态水放出热量61. 25 kJ,则该反应的热化学方程式为____。
(2)尾气中的NO2可以用烧碱溶液吸收的方法来处理,其中能生成NaNO2等物质,该反应的离子方程式为____。
(3)在773 K时,分别将2.00 mol N2和6.00 mol H2充入一个固定容积为1 L的密闭容器中发生反应生成NH3,气体混合物中c(N2)、c(H2)、c(NH3)与反应时间(t)的关系如图所示。
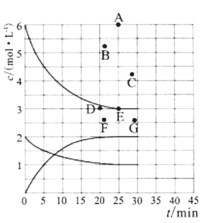
①下列能说明反应达到平衡状态的是____(选填字母)。
a.v正(N2)=3v逆(H2) b.体系压强不变
c.气体平均相对分子质量不变 d.气体密度不变
②在此温度下,若起始充入4. 00 mol N2和12. 00 mol H2,则反应刚达到平衡时,表示 c(H2)~t的曲线上相应的点为 ___(选填字母)。
(4)在373 K时,向体积为2L的恒容真空容器中充入0.40mol NO2,发生如下反应:![]()
测得NO2的体积分数[φ(NO2)]与反应时间(t)的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 |
φ(NO2) | 1.0 | 0.75 | 0.52 | 0.40 | 0.40 |
①计算0~20min时,v(N2O4)=____。
②已知该反应![]() ,其中k1、k2为速率常数,则373K时,
,其中k1、k2为速率常数,则373K时,![]() =_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
=_____;改变温度至T1时,k1=k2,则T1___ 373 K(填“>”“<”或“=”)。
【答案】2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ·mol-1 2NO2 + 2OH- = NO2-+ NO3 -+H2O bc B 2×103mol/(L·min) 60 >
【解析】
(1)根据题干信息计算反应热并书写热化学方程式;(2)根据氧化还原反应原理及题干信息书写反应方程式;(3)根据平衡状态的特点判断是否达到平衡状态,并用平衡移动原理及等效平衡思想分析解答;(4)由速率之比等于化学计量数之比计算反应速率,根据平衡常数的表达式及平衡移动原理分析解答。
(1)3.2g液态肼完全反应放出热量为61. 25 kJ,则2mol液态肼完全反应时放出的热量为:![]() ,则该反应的热化学方程式为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ·mol-1,故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ·mol-1;
,则该反应的热化学方程式为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ·mol-1,故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l) ΔH=-1225 kJ·mol-1;
(2)题干信息产物有NaNO2,根据氧化还原反应原理,N元素化合价既降低又升高,发生的是歧化反应,所以还有产物NaNO3,根据原子守恒判断产物中还有水,则反应方程式为:2NO2 + 2OH- = NO2-+ NO3 -+H2O,故答案为:2NO2 + 2OH- = NO2-+ NO3 -+H2O;
(3)①反应为:N2+3H2![]() 2NH3
2NH3
a.v正(N2) =1/3v正(H2)=3v逆(H2),正逆反应速率不相等,没有达到平衡状态,故错误; b.反应为气体体积减小的反应,体系压强不变,说明反应物和生成的浓度保持不变,反应达到平衡状态,故正确;
c.气体平均相对分子质量数值上等于气体总质量比上总物质的量,根据质量守恒反应前后气体总质量不变,平均相对分子质量不变,说明总物质的量不变,说明达到平衡状态,故正确;
d.气体总质量不变,体积不变,所以气体密度始终不变,不能说明达到平衡状态,故错误,故答案为:bc;
②起始充入4. 00 mol N2和12. 00 mol H2,相当于将充入2.00 mol N2和6.00 mol H2的两个容器“压缩”为一个容器,假设平衡不移动,根据图示分析知平衡时c(H2)=6mol/L,而“压缩”后平衡正向移动,则平衡时3mol/L <c(H2)<6mol/L,且达到平衡的时间缩短,故对应点为B,故答案为:B;
(4)①设20min时,反应掉的NO2为2x,则:
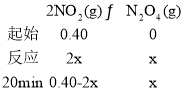
20min时,NO2的体积分数为0.75,所以![]() ,解得x=0.08,所以反应20min时,消耗NO2的物质的量为0.08×2mol=0.16mol,020min内,NO2的消耗速率为
,解得x=0.08,所以反应20min时,消耗NO2的物质的量为0.08×2mol=0.16mol,020min内,NO2的消耗速率为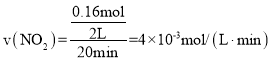 ,根据化学计量比等于反应速率之比,则v(N2O4)=1/2v(NO2)=2×103mol/(L·min),故答案为:2×103mol/(L·min);
,根据化学计量比等于反应速率之比,则v(N2O4)=1/2v(NO2)=2×103mol/(L·min),故答案为:2×103mol/(L·min);
②反应达到平衡时有v正=v逆,即v(NO2)=2v(N2O4),达到平衡时,NO2的体积分数为0.40,即![]() ,解得x=0.15,所以化学平衡常数为
,解得x=0.15,所以化学平衡常数为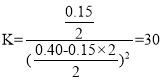 ,则有
,则有![]() ,所以
,所以![]() ;
;
改变温度至T1时k1=k2,由于k1=2K·k2,则K=![]() ,平衡常数减小,考虑到反应为放热反应,温度升高,不利于反应正向进行,所以温度应为升高,即T1>373K,故答案为:60;>。
,平衡常数减小,考虑到反应为放热反应,温度升高,不利于反应正向进行,所以温度应为升高,即T1>373K,故答案为:60;>。


科目:高中化学 来源: 题型:
【题目】在下列物质转化中,已知A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸;当X无论是强酸还是强碱时,都有如下的转化关系:

说明:当X是强酸时A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。(已知H2CO3、H2S、H2SO3、H2SiO3皆为二元弱酸)
请回答下列问题:
(1)A是___________,Y是___________,Z是____________(填化学式,下同)。
(2)当X是强酸时,E是_______________,写出B生成C的化学方程式:__________________。
(3)当X是强碱时,E是_______________,写出D生成E的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 17 g羟基(—OH)所含有的电子数是10NA个
B. 1 mol苯乙烯中含有的碳碳双键数为4NA个
C. 常温下,14 g乙烯和丙烯的混合物中总原子数为3NA个
D. 4.2 g C3H6中含有的碳碳双键数一定为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)===2H2O(l) ΔH=-570.0 kJ·mol-1;②CO(g)+![]() O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
O2(g)===CO2(g) ΔH=-280 kJ·mol-1。某H2和CO的混合气体完全燃烧放出141 kJ热量,同时消耗标准状况下5.6 L O2,则原混合气体中H2和CO的物质的量之比为( )
A.2∶1B.1∶2C.1∶1D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法处理酸性含铬废水(主要含有![]() )时,以铁板作阴、阳极,处理过程中存在反应
)时,以铁板作阴、阳极,处理过程中存在反应![]() +6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是 ( )
+6Fe2++14H+=2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去。下列说法不正确的是 ( )
A.阳极反应为Fe-2e-=Fe2+
B.电解过程中溶液c(H+)不会变化
C.处理过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有1 mol![]() 被还原
被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乳酸薄荷醇酯( ![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B.乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C.麦芽糖和纤维二糖水解后都只得到葡萄糖
D.检验某溶液中是否含有甲醛:在盛有2 mL 10%CuSO4溶液的试管中滴加0.5mL10%NaOH溶液,混合均匀,滴入待检液,加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(8分)A~G各物质间的关系如下图,其中B、D为气态单质。

请回答下列问题:
(1)物质C和E的名称分别为________________、__________________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_____________;
若只能在加热情况下进行,则反应物A应为_____________;
(3)反应②的化学方程式为_______________________________________;
(4)新配制的F溶液应加入_____________以防止其转化为G。检验G溶液中阳离子的常用试剂是_____________,实验现象为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用系统命名法给下列有机物命名:
CH3CH2C(CH3)2CH2CH3_________________________________________
化合物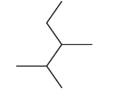 按系统命名法命名__________________________
按系统命名法命名__________________________
2,3-二甲基-4-乙基-2-庚烯的结构简式__________________________
(2)分子式为C4H8O2能发生水解反应的同分异构体有_____种,甲苯的一氯代物有______种。
(3)从某些植物树叶提取的挥发油中含有下列主要成分
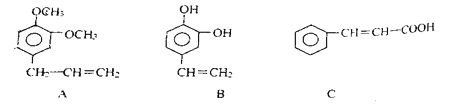
A的分子式是___________,B中的含氧官能团是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com