
 图中的曲线表示的是其他条件一定时,反应:2NO+O2?2NO2△H<0中N0的平衡转化率与温度的关系.图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是( )
图中的曲线表示的是其他条件一定时,反应:2NO+O2?2NO2△H<0中N0的平衡转化率与温度的关系.图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)<v(逆)的点是( )| A. | a点 | B. | b点 | C. | c点 | D. | d点 |
分析 在曲线上,当温度一定时,NO的转化率也一定,故曲线上任意一点都表示达到平衡状态,而曲线外的任意一点都表示未达平衡状态.在曲线下方的任意一点,要想达到同温度下的平衡状态,即向上引垂直线到曲线上的一点,这样NO的转化率要增大,平衡向右移动,在曲线上方的任意一点,要想达到同温度下的平衡状态,即向下引垂直线到曲线上的一点,这样NO的转化率要减小,平衡向左移动,据此解答.
解答 解:A、a点在曲线上方,未达到平衡状态,要想达到同温度下的平衡状态,即由d点向下引垂直线到曲线上的一点,这样NO的转化率要减小,平衡向左移动,故v(正)<v(逆),故A正确;
B、b点在曲线上,处于平衡状态,v(正)=v(逆),故B错误;
C、c点在曲线下方,未达到平衡状态,要想达到同温度下的平衡状态,即由c点向上引垂直线到曲线上的一点,这样NO的转化率要增大,平衡向右移动,故v(正)>v(逆),故C错误;
D、d点在曲线上,处于平衡状态,v(正)=v(逆),故D错误;
故选A.
点评 本题考查化学平衡图象,涉及平衡状态的判断、平衡移动等,难度中等,判断曲线上的任意一点都表示达到平衡状态是关键.


科目:高中化学 来源: 题型:选择题
| A. | 汽油车在行驶过程中,热能首先转化为化学能,化学能再转化为动能 | |
| B. | 炸药发生爆炸时化学能完全转化为热能 | |
| C. | 炭燃烧时化学能主要转化为光能 | |
| D. | 柴草燃烧时,部分化学能转化为热能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 需要加热才能发生的反应不一定是吸热反应 | |
| B. | 化学反应中的能量变化都表现为热量变化 | |
| C. | 向醋酸钠溶液中滴入酚酞试液,加热后若溶液红色加深,则说明盐类水解是吸热的 | |
| D. | 反应物和生成物所具有的总能量决定了反应是放热还是吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂 | B. | 改变压强 | ||
| C. | 适当提高反应温度 | D. | 将尾气点燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 少量双氧水滴入酸性KI溶液:2H2O2+2I-+4H+═4H2O+I2 | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | |
| D. | 碱性锌锰电池正极反应:2MnO2+2H2O+2e-═2MnOOH+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
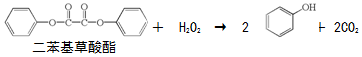
| A. | 上述反应是酯的水解反应 | |
| B. | 荧光棒发光过程涉及化学能到光能的转化 | |
| C. | 二苯基草酸酯苯环上的一氯代物共有4种 | |
| D. | 二苯基草酸酯与草酸( 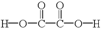 )互为同系物 )互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com