
合成可降解聚合物G的某流程的最后一步如下图,下列有关说法不正确的是
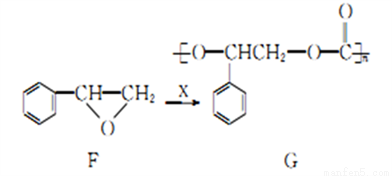
A. 已知该步转化过程中的原子利用率为100%,则X为CO2
B. 有机物F属于芳香族化合物,但不属于芳香烃
C. (C9H8O3)n既是高分子G的化学式也是其链节的化学式
D. 已知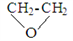 经水解生成乙二醇,则F、G在一定条件下水解,可得相同的产物
经水解生成乙二醇,则F、G在一定条件下水解,可得相同的产物
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:2017届全国新课程高考仿真信息理综(一)化学试卷(解析版) 题型:填空题
新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为 ,该能层具有的原子轨道数为 .
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是 ,B原子的杂化轨道类型是 .
Li、B、H元素的电负性由大到小排列顺序为 .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+ H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是 (填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为 ,NaH的理论密度是 g•cm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:选择题
短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是( )
A. 元素W、X的氯化物中,各原子均满足8电子的稳定结构
B. 元素X与氢形成的原子比为1:1的化合物有很多种
C. 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D. 元素Z可与元素X形成共价化合物XZ2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高一3月月考化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。下列有关叙述正确的是
A.大气雾霾污染现象的产生与汽车尾气排放有关
B.玻璃和氮化硅陶瓷都属于新型无机非金属材料
C.空气中的臭氧对人体健康有益无害
D.活性炭与二氧化硫都可用于漂白,其漂白原理相同
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(三)化学试卷(解析版) 题型:简答题
黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量的FeO、Fe2O3)生产硝酸铜溶液的流程如下:
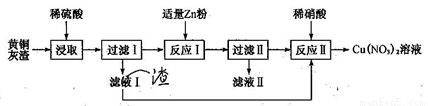
(1)写出酸浸时Fe2O3和稀硫酸反应的离子方程式:_________________。
(2)反应I中所加Zn不能过量的原因是________________。
(3)滤液II中含有的金属阳离子主要有_____________。
(4)写出反应II的离子方程式:______________。反应II应控制温度不能过高也不能过低的原因是___________________。
(5)已知Cu(NO3)2·6H2O和Cu(NO3)2·3H2O的溶解度随温度的变化如图所示。则由A点对应的溶液获取Cu(NO3)2·3H2O的方法是_______________。
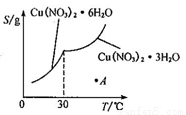
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(三)化学试卷(解析版) 题型:选择题
实验室用粗铜制取NO2并冋收硝酸铜晶体[Cu(NO3)2•3H2O],下列装置能达到实验目的的是
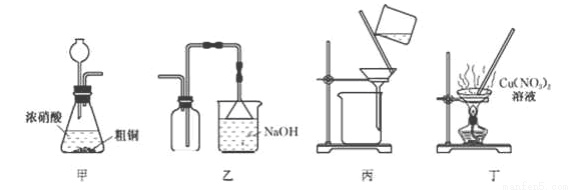
A. 用装置中制备NO2 B. 用装置乙收集NO2
C. 用装置丙过滤除去固体杂质 D. 装置丁蒸发至干得纯净硝酸铜晶体
查看答案和解析>>
科目:高中化学 来源:2017届天津市部分区高三质量调查(一)化学试卷(解析版) 题型:实验题
SnCl4是一种重要的工业原料,常作媒染剂等。已知SnCl4常温下是无色液体,在潮湿空气中易水解,熔点-36℃,沸点114℃。工业上制备SnCl4的工艺流程如下:
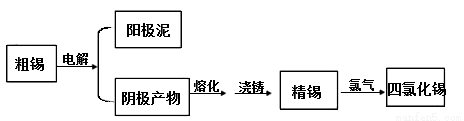
请回答下列问题:
(1)粗锡电解精炼时,常用硅氟酸(化学式为H2SiF6)和硅氟酸亚锡(化学式为SnSiF6)为电解液。已知H2SiF6为强酸,则用硅氟酸溶解氧化亚锡的离子方程式为______。硅氟酸有腐蚀性,能与SiO2反应。电解时可选取下列电解槽中的________。
a.玻璃电解槽 b.不锈钢电解槽 c.塑料电解槽
阴极发生的电极反应式为_________。
(2)某同学模拟工业制法设计了由Sn与Cl2反应制取SnCl4的实验装置如下:
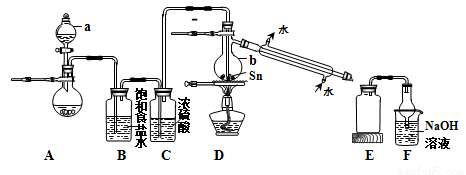
①a中浓盐酸与烧瓶内固体反应生成Cl2,则烧瓶内固体可以选用_________;仪器b的名称为_________。
②装置D的主要缺点是___________;除此之外,整套装置还有的缺点是_______。
③SnCl4溶液中加入适量的NaOH溶液,产生白色沉淀(二元酸),再加过量的NaOH溶液,白色沉淀溶解。试写出反应生成白色沉淀的离子方程式_________。
④若实验中取用锡粉5.95 g,反应后,E中广口瓶里收集到12.0 g SnCl4。则SnCl4的产率为_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市高二3月月考化学试卷(解析版) 题型:选择题
乙醇分子结构中的各种化学键如图所示,下列关于乙醇在各种反应中断键的说法正确的是
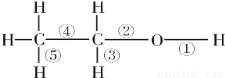
A.与醋酸、浓硫酸共热时断裂①
B.在空气中燃烧时断裂④⑤
C.和金属钠反应时断裂②
D.在Cu催化下和O2反应时断裂②③
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(四)化学 试卷(解析版) 题型:简答题
硼氢化钠(NaBH4)广泛用于精细有机合成。Bayer法合成硼氢化钠流程图如下:

(1)“合成”时,可在图甲所示的反应釜中进行。
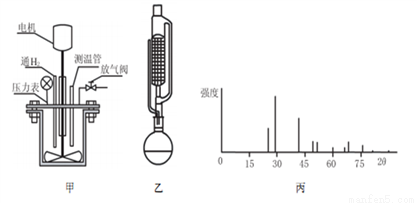
①从煤油中取出金属钠需先用滤纸吸干,再用石油醚洗涤,其目的是_______________。
②通氢气前需先通入氮气的目的是___________________。
③合成反应的化学方程式为________________________________。
(2)“萃取”时,可在图乙中进行,该仪器名称为_________________ 。
(3)实验中可以循环使用的物质是___________________;对所得产品进行分析得图丙图谱,该图谱名称为________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com