
分析 (1)由C(s)+O2(g)═CO2(g);△H1=-393.5kJ•mol-1可知,C的标准燃烧热是393.5kJ•mol-1;
(2)根据盖斯定律,①-②-③得到C(s)+H2O(g)=CO(g)+H2(g)△H;
(3)C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ•mol-1>0,反应物的总能量小于生成物的总能量;
(4)固体煤经处理变为气体燃料后,根据气体燃料具有的优点分析,煤通过途径Ⅱ作为燃料的意义是固体煤经处理变为气体燃料后,不仅在燃烧时可以大大减少SO2和烟尘对大气造成的污染,而且燃烧效率高,也便于输送;
解答 解:(1)由C(s)+O2(g)═CO2(g);△H1=-393.5kJ•mol-1可知,C的标准燃烧热是393.5kJ•mol-1,
故答案为:393.5;
(2:①C(s)+O2(g)═CO2(g);△H1=-393.5kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g);△H2=-241.8kJ•mol-1
③CO(g)+$\frac{1}{2}$O2(g)=CO2(g);△H3=-283.0kJ•mol-1
根据盖斯定律,①-②-③得到:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ•mol-1,
故答案为:C(s)+H2O(g)=CO(g)+H2(g)△H═+131.3kJ•mol-1;
(3)C(s)+H2O(g)=CO(g)+H2(g)△H=+131.3kJ•mol-1>0,吸热反应中反应物的总能量小于生成物的总能量,
故答案为:<;
(4)A、根据盖斯定律,反应热只与始态与终态有关,与途径无关,始态相同、终态相同反应热相同,途径1和途径2在理论上相同放出的热量相等,故A错误;
B.与途径Ⅰ相比,途径Ⅱ可以减少对环境的污染,固体煤经处理变为气体燃料后,不仅在燃烧时可以大大减少SO2和烟尘对大气造成的污染,故B正确;
C.与途径Ⅰ相比,途径Ⅱ可以提高煤的燃烧效率,固体煤经处理变为气体燃料后,与途径Ⅰ相比,途径Ⅱ可以提高煤的燃烧效率,故C正确
D.将煤转化为水煤气后,气体便于通过管道进行运输,故D正确.
故答案为:A.
点评 本题考查学生盖斯定律的应用以及反应吸放热与反应物、生成物能量之间的关系,注意盖斯定律的应用,题目难度不大.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
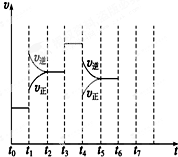 在一密闭容器中发生反应N2+3H22NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
在一密闭容器中发生反应N2+3H22NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
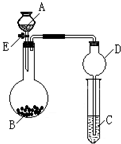 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 五价砷在维生素C作用下发生了还原反应 | |
| B. | “两者同食”发生的反应中维生素C作还原剂 | |
| C. | 河虾中含有的五价砷,没有毒性 | |
| D. | 毒药砒霜是含砷的氧化物,可以推测砒霜中所含的砷元素化合价为+5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH是氧化产物 | |
| B. | 当1molNaH发生反应时,该反应转移电子的物质的量为2mol | |
| C. | NaH为还原剂 | |
| D. | H2O既是还原剂又是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
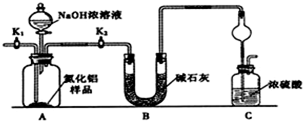
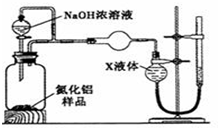
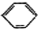
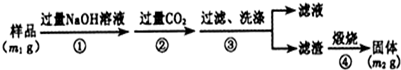
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2→MgO | B. | Fe3O4→H2O | C. | FeCl3→CuCl2 | D. | MnO2→Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
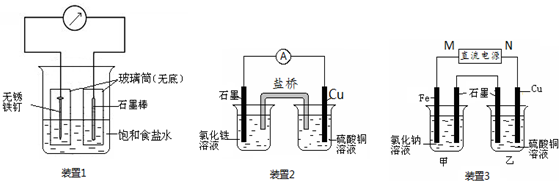
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com