
【题目】把200mL NH4HCO3和Na2CO3 的混合溶液分成两等份,取一份加入含amol NaOH的溶液恰好反应完全;取另一份加入含bmol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为
A. (l0b - 5a))mol/LB. (2b-a)mol/L
C. (![]() )mol/LD. (5b-
)mol/LD. (5b-![]() )mol/L
)mol/L
【答案】A
【解析】
NH4HCO3和Na2CO3的混合溶液加入NaOH,发生反应为:NH4HCO3+2NaOH═NH3![]() H2O+ Na2CO3+ H2O;
H2O+ Na2CO3+ H2O;
加入含b mol HCl的盐酸的反应为:NH4HCO3+HCl═NH4Cl+CO2↑+H2O,Na2CO3+2HCl═2NaCl+CO2↑+H2O,根据化学方程式计算解答。
设200mL溶液中含有NH4HCO3xmol,Na2CO3ymol,
NH4HCO3和Na2CO3的混合溶液加入NaOH反应为:
NH4HCO3+2NaOH═NH3![]() H2O+ Na2CO3+ H2O,
H2O+ Na2CO3+ H2O,
1 2
x amol
计算得出:x=0.5amol;故:NH4HCO3为0.5amol;
加入含b mol HCl的盐酸的反应为:
NH4HCO3+HCl═NH4Cl+CO2↑+H2O,
1 1
0.5amol n(HCl)
Na2CO3+2HCl═2NaCl+CO2↑+H2O,
1 2
y b-n(HCl)
计算得出:n(HCl)= 0.5amol,y=![]() (b- 0.5a) mol;
(b- 0.5a) mol;
n(Na+)=2n(Na2CO3)= (b- 0.5a) mol,c(Na+)=![]() =(5b-
=(5b-![]() )mol/L,
)mol/L,
所以D选项是正确的。


科目:高中化学 来源: 题型:
【题目】据调查,劣质的家庭装饰材料会释放出近百种能引发疾病的有害物质,其中一种有机物分子的球棍模型如右图,图中“棍”代表单键或双键或三键,不同大小的球代表不同元素的原子,且三种元素位于不同的短周期。下面关于该有机物的叙述不正确的是( )

A. 有机物化学式为![]() B. 分子中所有原子在同一个平面内
B. 分子中所有原子在同一个平面内
C. 该有机物难溶于水![]() D. 可由乙炔和氯化氢加成得到
D. 可由乙炔和氯化氢加成得到
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(可供选用的反应物只有CaCO3固体、6 mol·L1硫酸、6 mol·L1盐酸和蒸馏水)

回答下列问题:
(1)装置A中发生反应的化学方程式是______________________________________。
(2)装置B的作用是______________,装置C的作用是______________,装置E的作用是_____________。
(3)装置D中发生反应的化学方程式是______________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素X的气态氢化物与该元素最高价氧化物的水化物反应生成盐,则该元素
A. 在周期表中处于第三周期ⅦA族 B. 在周期表中处于第二周期ⅤA族
C. 氢化物稳定性比PH3弱 D. 常见化合价只有-3、+2、+3、+5价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数的值,下列叙述正确的是( )
A. 常温常压下,1.06g Na2CO3含有的Na+离子数为0.01 NA
B. 标准状况下,22.4LH2O含有的分子数为1 NA
C. 通常状况下,1 NA 个CO2分子占有的体积为22.4L
D. 标准状况下,22.4LH2与O2的混合气体所含分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摩拜单车利用车篮处的太阳能电池板向智能锁中的锂离子电池充电,电池反应原理为LiCoO2 +6C![]() li1-xCoO2 +lixC6,结构如图所示。下列说法正确的是
li1-xCoO2 +lixC6,结构如图所示。下列说法正确的是
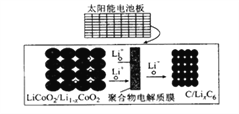
A. 放电时,正极质量增加
B. 充电时,锂离子由右向左移动
C. 该钾离了电池工作时,涉及到的能量形式有3 种
D. 充电时、阳极的电极反应式为Li1-xCoO2+xLi++xe-= LiCoO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如下图所示。则下列离子组在对应的溶液中,一定能大量共存的是( )

A. a点对应的溶液中:Na+、OH-、SO![]() 、NO
、NO![]()
B. b点对应的溶液中:Al3+、Fe3+、MnO![]() 、Cl-
、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO![]() 、Cl-
、Cl-
D. d点对应的溶液中:F-、NO![]() 、Fe3+、Ag+
、Fe3+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物和足量的银氨溶液在微热条件下发生银镜反应,生成10.8 g银,而燃烧等量的有机物时,需消耗氧气6.16 L(标准状况),该有机物是( )
A. 葡萄糖 B. 甲酸乙酯 C. 丁醛 D. 乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是( )
A. 元素Y、Z、W形成的离子具有相同电子层结构,其离子半径依次增大
B. 39g Z2Y2中含有的离子数约为1.204×1024
C. 元素Z、R的最高价氧化物的水化物之间相互反应生成的盐一定是正盐
D. 元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com