
| A. | M<N | B. | 2M=N | C. | N<M | D. | M=N |
分析 该反应是气体体积增大的化学反应,增大压强,平衡向逆反应方向移动,根据压强对化学平衡的影响分析判断.
解答 解:根据PV=nRT知,R为常数,当V、T相同时,n越大,P越大;该反应是气体体积增大的反应,当投入的物质的量加倍时,则相当于增大压强,平衡向气体体积减小的方向移动,即逆反应方向移动,所以导致反应达到平衡时PCl5的转化率减小,PCl5的体积分数增大,则盛有amolPCl5,达平衡时,PCl5所占体积分数为M%大于0.5amolPCl5反应达平衡时,PCl5所占体积分数为N%,故N<M.
故选C.
点评 本题考查了外界条件对化学平衡的影响,难度中等,正确运用等效平衡是解本题的关键.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
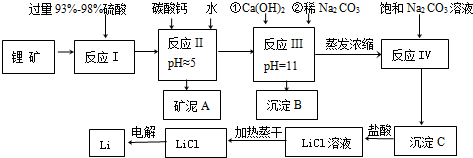
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH═5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.下列说法中正确的是( )
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示.先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH═5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解.下列说法中正确的是( )| A. | 电解过程中OH-从a极区通过离子交换膜c进入b极区 | |
| B. | 随着电解进行,KOH溶液浓度会逐渐减小 | |
| C. | 当阳极有0.1mol I-放电时,阴极生成6.72LH2 | |
| D. | a电极反应式:I--6e-+6OH-═IO3-+3H2O,a极区的KI最终转变为KIO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 4:1 | B. | 1:2 | C. | 2:1 | D. | 1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;再加入无水酒精又看到的现象是
;再加入无水酒精又看到的现象是查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com