
能正确表示下列反应的离子方程式的是
A.NaOH溶液中加入铝片:Al+2OH-=AlO2-+H2↑
B.NaHCO3溶液水解:HCO3-+H2O H3O+ +CO32-
H3O+ +CO32-
C.NH4HCO3溶液与足量烧碱溶液混合:HCO3-+OH-=CO32-+H2O
D.硫酸溶液与氢氧化钡溶液混合:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱。请写出电极反应式,负极________________________________________________________________________,
正极_____________________________________________________________________,
并在方框内画出实验装置图,要求用烧杯和盐桥,并标出外电路电子流向。
查看答案和解析>>
科目:高中化学 来源: 题型:
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是
A. N2H4+
N2H4+ O2===
O2=== N2+H2O ΔH=-267 kJ·mol-1
N2+H2O ΔH=-267 kJ·mol-1
B.N2H4(g)+O2(g)===N2(g)+2H2O(l) ΔH=-133.5 kJ·mol-1
C.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=+534 kJ
D.N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-534 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
往容积为10 L的密闭容器内通入40 mol N2和120 mo l H2,在一定条件下进行反应,经2s后达到平衡状态,平衡时c(N2)为2 mol/L。
l H2,在一定条件下进行反应,经2s后达到平衡状态,平衡时c(N2)为2 mol/L。
(1)用H2的浓度变化表示2 s内的平均速率v(H2)=__________。
(2)氮气的转化率是__________ 。
(3)平衡时混合气体中氨的体积分数是__________ 。
(4)反应开始与平衡时的压强之比是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学键与晶体结构说法正确的是
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物的高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.同一主族元素的气态氢化物,其相对分子质量越大,对应的熔、沸点一定越高
B.升高温度可加快反应速率,其主要原因是反应物分子能量增加,单位体积活化分子的数目增多,活化分子的百分数不变,使得有效碰撞次数增多
C.若R2-离子和M+离子的电子层结构相同,则原子序数:R>M
D.若弱酸HA的酸性强于弱酸HB,则同浓度钠盐溶液的pH:NaA<NaB
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24L苯中含有的C-H键的数目为0.6NA
B.标准状况下,由H2O2分解制得4.48LO2转移的电子数目为0.8NA
C.14 g 由乙烯与环丙烷(C3H6)组成的混合气体含有的碳原子数目为NA
D.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA
查看答案和解析>>
科目:高中化学 来源: 题型:
若不断地升高温度,实现“雪花―→水―→水蒸气―→氧气和氢气”的变化。在变化的各阶段被破坏的微粒间的相互作用依次是 ( )
A.氢键;分子间作用力;非极性键 B.氢键;分子间作用力;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
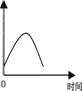
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率速率
可由右上图表示。在下列因素中对产生H2速率有影响的是
①盐酸的浓度 ②镁条的表面积 ③溶液的温度 ④Cl-的浓度
A.①④ B.③④ C.①②③ D.②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com