
(1)根据最新“人工固氮”的研究报道,在常温、光照条件下,N2在催化剂(掺有少最Fe2O3的TiO2)表面与水发生下列反应:N2(g)+3H2O(g) 2NH3(g)+3/2O2(g) △H =aJ/mol,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
2NH3(g)+3/2O2(g) △H =aJ/mol,进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
T/K | 303 | 313 | 323 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
此合成反应的a________0;△s _________0(填“>”、“<”或“=” )
(2)己知:常温下,0.1mol/L的某酸H2A的pH=4,则该酸为________酸(填“强”或“弱”)。H2A的电离方程式为______________,该滚液中由水电离出的c(H+)=______________。
(3)25℃时,0.1mol/L的HA溶液中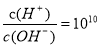 。0.010.1mol/L的BOH溶液pH=12,请回答下列问题:
。0.010.1mol/L的BOH溶液pH=12,请回答下列问题:
①HA是__________(填”强电解质”或“弱电解质”,下同)。
②在加水稀释HA的过程中,随着水量的增加而减小的是__________(填字母)。
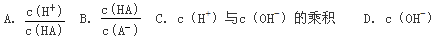
③在体积相等、pH相等的HA溶液与盐酸溶液中加入足量Zn,HA溶液中产生的气体比盐酸中产生的气体__________(填“多”“ 少”或“ 相等”)。
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源:2017届河北省高三上10.6周测化学试卷(解析版) 题型:选择题
pH=2的两种一元酸x和y,体积均为100ml,稀释过程中pH与溶液体积的关系如图所示,分别滴加NaOH溶液(c=0.1mol/L)至pH=7,消耗NaOH溶液的体积为Vx,Vy,则

A.x为弱酸Vx<Vy B.x为强酸Vx>Vy C.y为强酸Vx>Vy D.y为弱酸Vx<Vy
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月月考化学卷(解析版) 题型:填空题
2014年我国的冶金行业深受经济危机的冲击,尤其是Al、Fe的价格下滑幅度很大。请完成下面问题:
(1)冶炼后的铝渣中含有大量的硅酸铝钙(Al2Ca2Si5O15),可作耐火纤维的原料。硅酸铝钙用氧化物形式表示为______________________。
(2) 由下列物质冶炼相应金属时采用电解法的是 。
a. Fe2O3 b. NaCl c. Cu2S d. Al2O3
(3)高铁电池具有容量高、安全性能好和价格低廉等特点,如图是高铁电池的实验装置。
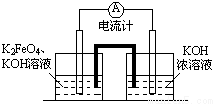
已知:放电后两极得到相同价态铁的化合物。
①电池放电时正极发生的电极反应式是______________________。
②若该电池属于二次电池,则充电时阴极的电极反应式为_______________________。
③已知盐桥中含有饱和KCl溶液,放电时,盐桥的作用是_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月月考化学卷(解析版) 题型:选择题
氢气用于烟气的脱氮、脱硫的反应 4H2(g)+2NO(g)+ SO2(g) 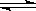 N2(g)+S(l)+4H2O(g) ΔH﹤0 。下列有关说法正确的是
N2(g)+S(l)+4H2O(g) ΔH﹤0 。下列有关说法正确的是
A.当v(H2)= v(H2O)时,达到平衡
B.升高温度,正反应速率减小,逆反应速率增大,化学平衡逆向移动
C.使用高效催化剂可提高NO的平衡转化率
D.化学平衡常数表达式为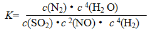
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月月考化学卷(解析版) 题型:选择题
下列有关说法正确的是
A.钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生
B.镀锌铁制品镀层受损后,铁制品比受损前更容易生锈
C.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g) ΔH<0,则该反应一定能自发进行
D.电解法精炼铜时,以粗铜作阳极,粗铜中的所有金属都以离子的形式进入电解质溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上9月月考化学卷(解析版) 题型:选择题
下列表示物质变化的化学用语正确的是( )
A.碳酸的电离H2CO3  2H++CO32-
2H++CO32-
B.氯化铁水解Fe3++3H2O Fe(OH)3+3H+
Fe(OH)3+3H+
C.硫氢化钠的水解HS-+H2O S2-+ H3O +
S2-+ H3O +
D.硫化铝固体在水中不存在Al2S3+6H2O Al(OH)3+3H2S
Al(OH)3+3H2S
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高二上第一次月考化学卷(解析版) 题型:选择题
下列属于油脂的用途的是( )
①人类的营养物质 ②制取肥皂 ③制取甘油 ④制备汽油.
A.①②④ B.①③⑤ C.②③④⑤ D.①②③
查看答案和解析>>
科目:高中化学 来源:2017届重庆市高三上定时训练(七)化学试卷(解析版) 题型:填空题
银铜合金广泛用于航空工业。从切割废料中回收并制备铜化工产品的工艺如下:
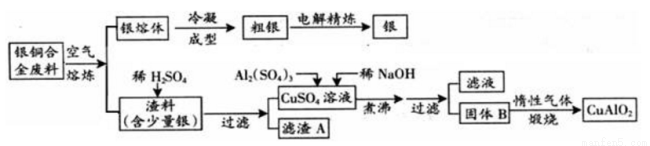
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为 ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式: CuO+ Al2O3 CuAlO2+ ↑。
CuAlO2+ ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 molCuAlO2,至少需要1.0mol·L-1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
向150ml 1mol/LNaOH溶液中通入标准状况下的CO2气体2.24L,待完全反应后,有关溶液中离子浓度的关系不正确的是
A.2c(OH-) + c(CO32-)=c(HCO3-) + 2c(H+) + 3c(H2CO3)
B.c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
C.c(Na+)>c(HCO3-)=c(CO32-)>c(H+)>c(OH-)
D.c(Na+)+ c(H+)=c(HCO3-) + 2c(CO32-) +c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com