
ij��ѧ�����ö������棨CeO2����̫���������½�H2O��CO2ת���H2��CO����������£�
mCeO2 ��m��x��CeO2•xCe+xO2
��m��x��CeO2•xCe+xO2
��m��x��CeO2•xCe+xH2O+xCO2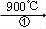 mCeO2+xH2+xCO
mCeO2+xH2+xCO
����˵������ȷ���ǣ� ��
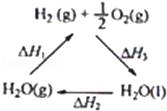
A���ù�����CeO2û������
B���ù���ʵ����̫������ѧ�ܵ�ת��
C��ͼ�С�H1=��H2+��H3
D����CO��O2���ɵļ���ȼ�ϵ�صĸ�����ӦʽΪCO+4OH����2e��=CO32��+2H2O

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ����Ͽ�и߶��µ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���Ӿ���������������ڷ��ӱ�����״��Ӱ�죬���ľ��彫ȡ�ܶѻ��ṹ��ԭ���Ƿ��Ӿ����У� ��
A�����Ӽ���������һ��������
B��ռ�ݾ����������ԭ��
C����ѧ���ǹ��ۼ�
D�����߶���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и߶����������ƻ�ѧ�Ծ��������棩 ���ͣ������
����������һ����ɫ����ζ�����Ҳ���ȼ�����壬�ڰ뵼��ӹ���̫���ܵ�������Һ����ʾ�������еõ��㷺Ӧ�ã�NF3��һ�������ͷ��ӣ�����102�㣬�е㩁129�棻����ͭ�Ĵ���������F2����NH3��Ӧ�õ���
��1��д���Ʊ� NF3�Ļ�ѧ��Ӧ����ʽ�� ��
��2��NF3�ķе��NH3�ķе㣨��33�棩�͵ö����Ҫԭ���� ��
��3��NF3��NԪ�ز�ȡ ��ʽ�ӻ���
��4��������HF��NaAlO2��NaCl��6��1��2�����ʵ���֮��ǡ�÷�Ӧ����HCl��H2O��һ������ˮ����Ҫԭ�ϣ������ʺ�������Ԫ�أ�������ʵĻ�ѧʽΪ �����������ǣ���λ��Ϊ ��
��5����֪����Ԫ�أ���O����S����Se����Te������ҵ�Ͽ���Al2Te3���Ʊ�H2Te��������л�ѧ����ʽ��
Al2Te3+ �T Al��OH��3��+ H2Te��
��6����֪�ڳ����£�����17g H2S�ų�56.1KJ����������д������ֽ���Ȼ�ѧ����ʽ ��
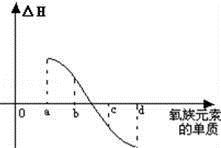
��7����ͼ��ʾΪ����Ԫ�ص�����H2��Ӧ�����е������仯ʾ��ͼ������a��b��c��d�ֱ��ʾ������ijһԪ�صĵ��ʣ���HΪ��ͬ���ʵ����ĵ�����H2��Ӧ�ķ�Ӧ�ȣ���b���� ��d���� ����д�������ƣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и߶����������ƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
x��yΪ����Ԫ�ص�ԭ�ӣ�x����������y�������Ӿ�����ͬ�ĵ��Ӳ�ṹ���ɴ˿�֪�� ��
A. x��ԭ�Ӱ뾶����y��ԭ�Ӱ뾶
B. x�ĵ縺�Դ���y�ĵ縺��
C. x�ĺ˵��������y�ĺ˵����
D. x�ĵ�һ������С��y �ĵ�һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и߶������л�ѧ�Ծ��������棩 ���ͣ������
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��
X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
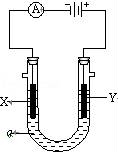
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ������X�������۲쵽��ʵ�������� ��Y�缫�ϵĵ缫��ӦʽΪ ����������ת�Ƶĵ���Ϊ0.2mol����X�缫�ϲ�������������� L����״���£���
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����X�缫�IJ����� ��Y�缫�ĵ缫��ӦʽΪ ����˵�������ʷ����ĵ缫��Ӧ����д����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ���¶��£����淴ӦX��g��+3Y��g��?2Z��g���ﵽ��Ӧ�ȵı�־�ǣ� ��
A��Z���������ʺ�X�ķֽ��������
B����λʱ��������n molX��ͬʱ������3n molY
C��X��Y��Z��Ũ�Ȳ��ٱ仯
D��X��Y��Z�ķ��Ӹ���֮��Ϊ1��3��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�����и߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڵ�ⱥ��ʳ��ˮ��Һ������������ȷ���ǣ� ��
A�����ʱ�������õ�������
B����������������Һ�е����̪��Һ����Һ�ʺ�ɫ
C�������������л���ɫ���������������ʹʪ����۵⻯����ֽ����
D�����һ��ʱ������Һȫ��ת�Ƶ��ձ��У���ֽ������Һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ�����и߶���4�¶ο���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����л����ڿ�����ȼ�յ�˵����ȷ���ǣ� ��
A. ֻ��̼���������ˮ
B. ֻ��CO2��ˮ
C. ������̼�������ˮ������Ԫ�صĻ�����
D. ��CO��CO2��ˮ������Ԫ�صĻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016���ֶ���ʦ����ʵ��ѧУ����ʵ��ѧУ�߶�����ĩ��ѧ���������棩 ���ͣ������
�±���ʵ����Ԫ�����ڱ��IJ��ֱ߽磬�����ϱ߽粢δ��ʵ������

������Ϣ�ش��������⣺
��1����̬Gaԭ�ӵ����������Ų�ʽΪ
��2����Ԫ��λ��Ԫ�����ڱ��� ����Fe��CO���γ������Fe��CO��5����Fe��CO��5�����Ļ��ϼ�Ϊ ��
��3����֪��ԭ����Ŀ�ͼ۵�����������ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������CO��Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ �� ���ѧʽ����
��4����CH4��CO��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ����� ��
��5������VSEPRģ��Ԥ��ED4���Ŀռ乹��Ϊ ��B��C��D��Eԭ��������γɵķ����У�����ԭ�Ӷ����������8�����ȶ��ṹ�ķ���Ϊ ��д2�֣���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com